下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:①一般认为H2SO4浓度大于
| 下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证: ①一般认为H2SO4浓度大于60%,就具有一定的强氧化性,越浓氧化性越强,60%以下的H2SO4主要体现的是酸性,基本上不体现强氧化性. ②温度也影响氧化性,如铜放于冷的浓H2SO4中反应不明显,如果加热就可以观察到明显现象. ③98%的浓H2SO4物质的量浓度为18.4mol/L,密度为1.84g?cm-3,根据以上信息回答: (1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓H2SO4 0.5mL,加热至沸腾,该试管中液体没有明显变化,试用数据解释原因______ (2)乙同学利用所示装置直接从分液漏斗中再加浓H2SO4 10mL与铜片反应.观察到右边试管中溶液褪色,这是因为______;若把品红试液换成硝酸酸化的硝酸钡溶液,产生的现象是______; 在左边试管中观察到的现象除了铜粉变黑色外,还有:①______,原因是______ ②有白色固体在试管底部析出,原因是______; (3)丙同学等乙同学实验结束后,取左试管(内有没反应完的铜)倾出上层清液于试管中来检验剩余的硫酸,他可以选择下列哪些试剂______(填写编号). A.锌粉 B.银粉 C.氯化钡溶液 D.碳酸氢钠溶液. 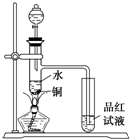 |
参考解答
(1)98%的浓H2SO4 0.5mL与3mL水混合后溶液的质量分数为
故答案为:H2SO4溶液的质量分数为23%<60%,其氧化性不强,所以无明显现象; (2)浓硫酸与铜在加热条件下发生氧化还原反应生成具有漂白性的二氧化硫和硫酸铜,二氧化硫可使品红褪色,二氧化硫具有还原性,可与硝酸发生氧化还原反应生成硫酸,若把品红试液换成硝酸酸化的硝酸钡溶液,可观察到由白色沉淀生成,反应后溶液呈蓝色,原因是溶液中含有铜离子,有白色固体在试管底部析出,原因是98%浓H2SO4有吸水性,生成无水CuSO4, 故答案为:生成具有漂白性的二氧化硫;由白色沉淀生成;液体呈浅蓝色;溶液中含有Cu2+;98%浓H2SO4有吸水性,生成无水CuSO4; (3)检验硫酸,可用活泼金属或碳酸氢钠,都有气体生成,但不能用银,因银与稀硫酸不反应,无论是否有硫酸剩余,加入氯化钡,都有沉淀生成,故答案为:AD. |
相似问题
设计了四种制备气体的方案:①加热稀硫酸和乙醇制备乙烯;②加热稀盐酸和二氧化锰制备氯气;③用稀硫酸和大
设计了四种制备气体的方案:①加热稀硫酸和乙醇制备乙烯;②加热稀盐酸和二氧化锰制备氯气;③用稀硫酸和大理石制备二氧化碳;④用稀硝酸和硫化亚铁制备
在生活 生产及化学研究中 人们经常需要根据不同原子 分子或离子的某些特征反应对物质进行区别 检验等.
在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行区别、检验等.下列说法正确的是( )A.用KOH溶液可以将
下列各组物质的溶液 分别只用一种试剂一次就可加以区别的是( )A.Na2SO4 BaC12 K2C
下列各组物质的溶液,分别只用一种试剂一次就可加以区别的是( )A.Na2SO4、BaC12、K2CO3、KNO3B.NaAlO2、NaC1、Na2CO3、AgNO3C.NaOH、KC1、K2CO3
下列四组溶液中 不用其它试剂即可全部鉴别的是( )①CuSO4 Na2SO4 BaCl2
下列四组溶液中,不用其它试剂即可全部鉴别的是( )①CuSO4Na2SO4BaCl2②NaHCO3Ba(OH)2H2SO4 ③HClNaOHNaHSO4 ④Ca(OH)2Na2CO3BaCl2.A.①②B.②③C.①③④D.①②④
某活动课程小组拟用50mL NaOH溶液吸收CO2气体 制备Na2CO3溶液.为了防止通入过量的CO
某活动课程小组拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:a.取25mLNaOH溶液吸收过量的












