某厂废水中含量金属Cr3+(含有少量Fe3+ Cu2+)。某研究性学习小组为了变废为宝 将废水处理得
某厂废水中含量金属Cr3+(含有少量Fe3+、Cu2+)。某研究性学习小组为了变废为宝,将废水处理得到重铬酸钾。某含铬废水处理的主要流程如图所示: 已知:①  沉淀完全,而在pH≥3.2时 沉淀完全,而在pH≥3.2时Fe(OH)3沉淀完全。 ②CrO2—4在酸性环境中发生:  回答下列问题: (1)滤渣的成分是 。(写化学式) (2)写出第③步反应的离子方程式 。 (3)分离出含[Cr(OH)4]—的溶液需要的玻璃仪器有 。 (4)目前一种采用以铬酸钾为原料,电化学法制备重要铬酸钾的实验装置示意图如下: 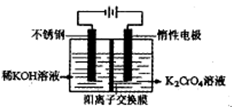 电解一段时间后,测定阳极液中K元素和Cr元素的含量,若K元素与Cr元素的物质的量之比 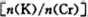 为d,则此时的铬酸钾的转化率为 。 为d,则此时的铬酸钾的转化率为 。 |
参考解答
| (1)Cr(OH)3、Fe(OH)3、Cu(OH)2(3分) (2)2[Cr(OH)4-+3H2O2+2OH-=2CrO42-+8H2O(2分) (3)漏斗、烧杯、玻璃棒(3分) (4)2-d(2分) |
试题分析:(1)由题干所给信息可知在pH=8.0~9.5时,Cr3+、Fe3+、Cu2+均转化为相应氢氧化物沉淀,因此利用流程可知滤渣的成分为Cr(OH)3、Fe(OH)3、Cu(OH)2。(2)在第③步中+3价Cr被氧化为+6价Cr,因此H2O2被还原,结合溶液为碱性和电荷守恒等可写出反应的离子方程式。(3)调节pH=13时,Cr(OH)3溶解,而Fe(OH)3、Cu(OH)2仍为固体,因此可通过过滤操作分离出[Cr(OH)4-,过滤操作所需玻璃仪器有玻璃棒、烧杯、漏斗。(4)由电解图示知电解时,阳极室发生反应为4OH--4e-=O2↑+2H2O,导致溶液中c(H+)增大,促使2CrO42- +2H+  Cr2O72-+H2O向右进行,同时K+移向阴极,因此可推知阳极室中CrO42-转化的物质的量等于电路中通过电子的物质的量,等于移向阴极K+的物质的量;而由原子守恒知电解前阳极液中n(K)/n(Cr)=2,电解后阳极液中n(K)/n(Cr)=d,故电解后阳极室中减少的n(K+)=n(Cr)转化=(2-d)×nCr,因此铬酸钾的转化率等于(2-d)×n(Cr)÷n(Cr)=2-d。 Cr2O72-+H2O向右进行,同时K+移向阴极,因此可推知阳极室中CrO42-转化的物质的量等于电路中通过电子的物质的量,等于移向阴极K+的物质的量;而由原子守恒知电解前阳极液中n(K)/n(Cr)=2,电解后阳极液中n(K)/n(Cr)=d,故电解后阳极室中减少的n(K+)=n(Cr)转化=(2-d)×nCr,因此铬酸钾的转化率等于(2-d)×n(Cr)÷n(Cr)=2-d。 |
相似问题
(12分)如下图 通电5 min后 电极5质量增加2.16 g 回答:(1)电源:a是_______
(12分)如下图,通电5 min后,电极5质量增加2 16 g,回答:(1)电源:a是________极,b是________极;A池电极反应,电极1:__________;电极2:_______
常温时 用某新型充电电池电解如右图所示的l00mL溶液 充电电池的总反应为4Li+2SOCl2 4
常温时,用某新型充电电池电解如右图所示的l00mL溶液,充电电池的总反应为4Li+2SOCl2 4LiCl +S+SO2,则下列叙述中不正确的是A.若仅闭合K2,铁极的电极
下图两个装置中 液体体积均为200mL 开始工作前电解质溶液的浓度均为0.5 mol·L-1 工作一
下图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0 5 mol·L-1,工作一段时间后,测得有0 02 mol电子通过,若忽略溶液体积的变化,
(16分)电解原理在化学工业中有广泛应用。右图表示一个电解池 装有电解液a;X Y是两块电极板(X
(16分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相
给你提供纯锌 纯铜片和500mL0.2mol·L-1的H2SO4溶液 导线 1000mL量筒。试用下
给你提供纯锌、纯铜片和500mL0 2mol·L-1的H2SO4溶液、导线、1000mL量筒。试用下图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。(












