如图所示为可逆反应A+2B2C+3D的化学反应速率随外界条件变化(先降温后加压)的关系图 由此可知(
如图所示为可逆反应A+2B 2C+3D的化学反应速率随外界条件变化(先降温后加压)的关系图,由此可知( ) 2C+3D的化学反应速率随外界条件变化(先降温后加压)的关系图,由此可知( )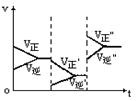 A.正向△H>0,B、C、D均为气体 B.正向△H<0,A、B、C为气体,D为液体或固体 C.正向△H>0,A、B为气体,D为液体或固体 D.正向△H<0,A为液体,C、D为气体 |
参考解答
| B |
| 根据图像可知,降低温度后,平衡向正反应方向移动,即正反应是放热反应。增大压强后,正逆反应速率均增大,说明反应物和生成物中一定都含有气体,由于平衡还是向正反应方向移动,说明正反应是体积减小的反应,所以B是正确的,答案选B。 |
相似问题
把0.6 mol X气体和0.4 mol Y气体混合于2 L容器中 使它们发生如下反应:3X(g)+
把0 6 mol X气体和0 4 mol Y气体混合于2 L容器中,使它们发生如下反应:3X(g)+Y(g)===nZ(g)+2W(g),在5 min时已经生成0 2 mol W,若测知以Z的
17..对于反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) 下列叙述不正确的
17. 对于反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述不正确的A.其反应物或生成物都能用来表示该反应的速率B.反应过程中能量关系可用上图表示
在2A+B 3C+4D反应中 表示该反应速率最快的是( )A.v(A)=0.5 mol&midd
在2A+B 3C+4D反应中,表示该反应速率最快的是( )A.v(A)=0 5 mol·L-1·s-1B.v(B)=0 3 mol·L-1·s-1C.v(C)=0 8 mol·L
已知:4NH3+5O2 4NO+6H2O 若反应速率分别用 [(mol / (L·min)]表示
已知:4NH3+5O24NO+6H2O,若反应速率分别用、、、[(mol (L·min)]表示,则正确的关系是 ( ) A.4=5B.5=6C.2=3D.4=5
某温度时 2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析 该反应的化学方程式
某温度时,2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均速率分别为A.3X+Y












