在一密闭体系中发生下列反应:N2(g)+3H2(g)2NH3(g)(正反应放热)如图是某一时间段中反
在一密闭体系中发生下列反应:N2(g)+3H2(g) 2NH3(g)(正反应放热)如图是某一时间段中反应速率与反应进程的曲线关系图,回答下列问题: (1)处于平衡状态的时间段是______. (2)t1、t3、t4时刻体系中分别是什么条件发生了变化? t1:______,t3:______,t4:______. (3)下列各时间段时,氨的体积分数最高的是______ A.t0~t1B.t2~t3C.t3~t4D.t5~t6. 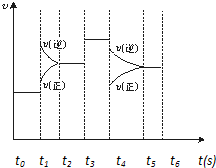 |
参考解答
| (1)从平衡状态的本质特征分析,可逆反应达到平衡时,正逆反应速率相等,时间处于t0~t1,t2~t3,t3~t4,t5~t6时,正逆反应速率相等,则说明反应达到平衡状态,故答案为:t0~t1,t2~t3,t3~t4,t5~t6; (2)t1时,正逆反应速率都增大,且逆反应速率大于正反应速率,反应向逆反应方向移动,则应为升高温度的变化, t3时,正逆反应速率都增大,正逆反应速率相等,平衡不移动,应为加入催化剂的变化, t4时,正逆反应速率都减小,且逆反应速率大于正反应速率,平衡向逆反应方向移动,由方程式计量数关系可知,应为减小压强的变化, 故答案为:升温;加催化剂;减压; (3)随着反应的进行,生成的氨气逐渐增多,氨气的体积分数逐渐增大,反应进行到最大时间时,生成的氨气最多,氨的体积分数最高,故答案为:A. |
相似问题
下列图象表达正确的是( )A.图①表示25℃时 用0.1mol?L-1盐酸滴定20mL0.1mol
下列图象表达正确的是( )A.图①表示25℃时,用0 1mol?L-1盐酸滴定20mL0 1mol?L-1NaOH溶液B.图②表示常温下,两份足量、等浓度的盐酸与等量锌粉反
能增加反应物分子中活化分子的百分数的是( )A.降低温度B.使用催化剂C.增大压强D.增加浓度
能增加反应物分子中活化分子的百分数的是( )A.降低温度B.使用催化剂C.增大压强D.增加浓度
用铁片与稀硫酸反应制取氢气时 下列措施不能使氢气生成速率加大的是( )A.加热B.不用稀硫酸 改用
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )A.加热B.不用稀硫酸,改用98%的浓硫酸C.滴加少量CuSO4溶液D.不用铁片,改用铁粉
以下实验能获得成功的是( )A.用乙醇和乙酸混合共热制取乙酸乙酯B.向H2O2溶液中滴加少量FeC
以下实验能获得成功的是( )A.用乙醇和乙酸混合共热制取乙酸乙酯B.向H2O2溶液中滴加少量FeCl3溶液,探究浓度对化学反应速率的影响C.向淀粉水解后
某学生为了探究锌与盐酸反应过程中速率变化.在100mL稀盐酸中加入足量的锌粉 标准状况下测得数据累计
某学生为了探究锌与盐酸反应过程中速率变化.在100mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下:时间(min)12345氢气体积(mL)5012023229












