已知可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O据此设计出如图所示的实验装置(
| 已知可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路).进行如下操作: (Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安表指针偏转; (Ⅱ)若改向(B)烧杯中滴加40%NaOH溶液,发现微安表指针向前述相反方向偏转. 试回答下列问题: (1)两次操作过程中微安表指针为什么会发生偏转?______ (2)两次操作过程中指针偏转方向为什么相反?______ (3)(Ⅰ)操作过程中,C1棒发生的反应为______ (4)(Ⅱ)操作过程中,C2棒发生的反应为______. 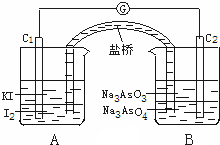 |
参考解答
| 由图可知,该装置为原电池,(Ⅰ)发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,电极反应发生2I--2e-=I2; (Ⅱ)发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极, (1)因两次操作过程均能形成原电池,都是把化学能转化为电能,形成电流指针偏转,故答案为:两次操作过程均能形成原电池,都是把化学能转化为电能; (2)因操作1中C1是负极,C2是正极;操作2中C1是正极,C2是负极,电子由负极流向正极,则指针偏转方向不同, 故答案为:操作1中C1是负极,C2是正极;操作2中C1是正极,C2是负极; (3)C1棒为负极,电极反应发生2I--2e-=I2,故答案为:2I--2e-=I2; (4)C2棒为负极,电极反应为AsO33-+H2O-2e-=AsO43-+2H+,故答案为:AsO33-+H2O-2e-=AsO43-+2H+. |
相似问题
把a b c d四块金属浸泡在稀硫酸中 用导线两两相连 可组成各种原电池 若a b相连时 a为负极;
把a、b、c、d四块金属浸泡在稀硫酸中,用导线两两相连,可组成各种原电池,若a、b相连时,a为负极;c、d相连时,d上有气泡冒出;a、c相连时,c为正极;b
已知稀H2SO4的浓度相等 有下列两种装置如图 下列说法正确的是( )A.a b均为原电池B.c
已知稀H2SO4的浓度相等,有下列两种装置如图,下列说法正确的是( )A.a、b均为原电池B.c、d均为电解池C.b池中Fe极反应为Fe-2e-═Fe2+D.d池中Cu极
如图为一原电池装置 下列叙述中正确的是( )A.铜是阳极 铜片上有气泡产生B.盐桥中的K+移向Zn
如图为一原电池装置,下列叙述中正确的是( )A.铜是阳极,铜片上有气泡产生B.盐桥中的K+移向ZnSO4溶液C.电流从锌片经导线流向铜片D.铜离子在铜片
如图是一个化学过程的示意图.已知甲池的总反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2
如图是一个化学过程的示意图.已知甲池的总反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O请回答:(1)甲池是______池,通入O2的电极作为______极,电极反应式为
一氧化碳是一种用途相当广泛的化工基础原料。(1)利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍
一氧化碳是一种用途相当广泛的化工基础原料。(1)利用下列反应可以将粗镍转化为纯度达99 9%的高纯镍:则该反应的△H0(选填“>” 或“<”)。(2)在高












