对于反应N2O4(g) 2NO2(g)在温度一定时 平衡体系中NO2的体积分数ψ(NO2)随压强的
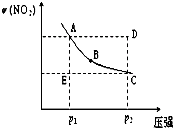
对于反应N2O4(g)  2NO2(g)在温度一定时,平衡体系中NO2的体积分数ψ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是( )
 |
参考解答
| A、增大压强,反应速率增大,C点压强大于A点压强,所以v(A)<v(C),故A正确; B、处于曲线上的状态为平衡状态,E点NO2的物质的量少于平衡状态时的物质的量,反应应向生成NO2的方向移动,此时v(正)>v(逆),D点NO2的物质的量多于平衡状态时的物质的量,反应向逆反应方向移动,此时v(正)<v(逆),故B错误; C、压强越大,反应速率越大,达到平衡状态时用的时间越少,E→A和D→C的物质的量相等,应为x>y,故C错误; D、从p1突然加压至p2,瞬间平衡没有移动,NO2的体积分数不变,再缓慢降压时,平衡向正反应方向移动,NO2的体积分数逐渐增大,故D正确. 故选AD. |
相似问题
下列说法中正确的是( )A.化学平衡常数越大 说明该反应进行得越完全B.可逆反应达到化学平衡状态后
下列说法中正确的是( )A.化学平衡常数越大,说明该反应进行得越完全B.可逆反应达到化学平衡状态后,改变外界条件不会改变平衡状态C.化学反应中,
某温度下 向容积为2L的密闭反应器中充入0.10 mol SO3 当反应器中的气体压强不再变化时测得
某温度下,向容积为2L的密闭反应器中充入0 10molSO3,当反应器中的气体压强不再变化时测得SO3的转化率为20%,则该温度下反应2SO2(g)+O22SO3(g)的平衡常
下列关于反应限度的叙述不正确的是 [ ]A.反应限度是一种平衡状态 此时反应已经
下列关于反应限度的叙述不正确的是 [ ]A.反应限度是一种平衡状态,此时反应已经停止 B.达到平衡状态时,正反应速率和逆反应速率相等 C.达到平衡状
关于平衡常数 下列说法不正确的是( )A.平衡常数不随反应物或生成物的浓度的改变而改变B.平衡常数
关于平衡常数,下列说法不正确的是( )A.平衡常数不随反应物或生成物的浓度的改变而改变B.平衡常数随温度的改变而改变C.平衡常数随压强的改变而改
对于可逆反应 SO2(g)+O2(g)SO3(g) △H
对于可逆反应,SO2(g)+O2(g)SO3(g) △H<0在一定温度下其平衡数为K 下列说法正确的是[ ]A.增大SO2的转化率K值一定增大 B.减小压强K值减小 C.升高












