(6分)(1)X Y Z三种金属 X Y组成原电池 X是负极;把Y放在Z的硝酸盐溶液中 Y表面有Z析
| (6分)(1)X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸盐溶液中,Y表面有Z析出。其活泼顺序是_________________; (2)由氢气和氧气反应生成1mol水蒸气放热241.8 kJ,写出该反应的热化学方程式:___________________________ _______。 (3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是 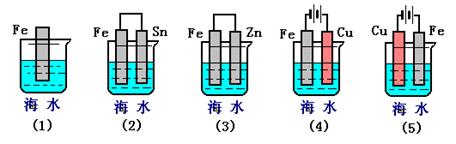 |
参考解答
| (1)X>Y>Z (2)2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol-1 (3) ⑸⑵⑴⑶⑷ |
| (1)在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。X、Y组成原电池,X是负极,因此X的金属性强于Y;Y放在Z的硝酸盐溶液中,Y表面有Z析出,则Y的金属性强于Z,所以金属性强弱顺序是X>Y>Z。 (2)氢气和氧气反应生成1mol水蒸气放热241.8 kJ,所以该反应的热化学方程式是)2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol-1。 (3)根据装置图可知,(1)装置是铁的化学腐蚀,(2)、(3)是原电池,其中(2)中铁是负极加速腐蚀,(3)中铁是正极,被保护;(4)、(5)是电解池,其中(4)中铁是阴极,被保护,(5)中铁是阳极,失去电子,加快腐蚀,所以铁片腐蚀由快到慢的顺序是⑸⑵⑴⑶⑷。 |
相似问题
碱性电池具有容量大 放电电流大的特点 因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液 电池总
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l) ==Zn(OH)2(s
碱性电池具有容量大 放电电流大的特点 因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液 电池总
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+
镍镉可充电电池在现代生活中有广泛应用 它的充 放电反应按下式进行:由此可知 该电池放电时的负极是 [
镍镉可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:由此可知,该电池放电时的负极是 [ ]A.CdB.NiOOH C.Cd(OH)2D.Ni(OH)2
铅蓄电池的两极分别为Pb PbO2 电解质溶液为H2SO4 工作时的反应为 Pb+PbO2+2H2S
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为 Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论不正确的是 [ ]A Pb为负极被氧化 B 外
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下左图所示。下列说法中 正确的是A.若a极是铜 b
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下左图所示。下列说法中,正确的是A.若a极是铜,b极为铁时,当电池消耗1 6g O2,b极上析出6 4g铜B












