(12分)为探究铁与浓硫酸在加热条件下的反应 某活动小组设计并完成以下实验:(1)实验目的:分析铁与
(12分)为探究铁与浓硫酸在加热条件下的反应,某活动小组设计并完成以下实验: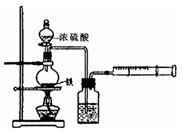 (1)实验目的:分析铁与浓硫酸在加热条件下的反应。 ①洗气瓶中浓硫酸的作用是 。 ②写出加热条件下铁与浓硫酸反应生成SO2的化学方程式 。 活动小组预测随着反应的进行,硫酸的浓度降低,可能还会有氢气产生,为进一步确认气体的成分还需要进行进一步的实验。 (2)实验目的:检验气体的成分。 试剂:氢氧化钠溶液、浓硫酸、氧化铜粉末、无水硫酸铜固体、品红溶液、高锰酸钾酸性溶液、碱石灰。 仪器如下图(可重复使用,可根据需要取用); 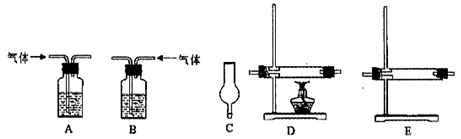 ①连接仪器。将装置的字母填入□内,并将试剂名称填写在相应的括号内(可不填满) 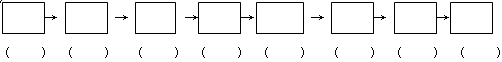 ②若混合气体中含有氢气,实验过程中能观察到的现象是 。 (3)实验目的:确定产物的含量。 ①若混合气体中含有SO2和H2,为测定混合气体中各成分含量,需收集的数据有 。 ②若反应后烧瓶中溶液含有的金属阳离子有Fe2+、Fe3+,其中检验是否含有Fe2+可采用的试剂为 ;如果该过程中共消耗了11.2g铁,反应后的溶液能吸收标准状况下1.12L氯气,则原溶液中含有Fe3+的物质的量为 mol。 |
参考解答
| (12分) (1)① 干燥气体 ② 2Fe+6H2SO4(浓)△Fe2(SO4)3+3SO2↑+6H2O (2)① A-A-A(或C)-D-E-A(或C)或A-A-A-A(或C)-D-E-A(或C)(合理给分) 品红溶液——高锰酸钾酸性溶液—浓硫酸(或石灰)—氧化铜粉末—无水硫酸铜固体—浓硫酸  碱石灰 碱石灰或:品红溶液—高锰酸钾酸性溶液—高猛酸钾酸性溶液(或品红)—浓硫酸(或碱石灰)—氧化铜粉末—无水硫酸铜固体—浓硫酸或碱石灰 或:品红溶液—氢氧化钠溶液—高猛酸钾酸性溶液(或品红)—浓硫酸(或碱石灰)—氧化铜粉末—无水硫酸铜固体—浓硫酸或碱石灰 ② D中固体粉末由黑色变为红色,E中固体由白色变为蓝色 (3)①混合气体的总体积、反应前后D中粉末质量的差值(反应前D中氧化铜粉末质量反应后D中粉末的质量)(其他合理给分) ② 酸性高锰酸钾溶液 、 0.1 |
| 略 |
相似问题
(11分)某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法 研究影响反应
(11分)某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。(1)实验条件作如下限定:所用KMnO4酸性溶液的
(I)(4分)为了探究苯酚和乙醇分子中羟基上氢原子的活泼性 甲 乙两位同学分别设计如下甲 乙两方案。
(I)(4分)为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计如下甲、乙两方案。方案甲:实验1:取少量无水乙醚于试管中,加入少
已知某白色混合物粉末中含有CuSO4 K2SO4 NH4HCO3 NH4Cl NaCl五种物质中的两
已知某白色混合物粉末中含有CuSO4、K2SO4、NH4HCO3、NH4Cl、NaCl五种物质中的两种,且物质的量之比为1:1。请完成下述探究混合物组成的实验。限选的仪器、
为了粗略测定电石中碳化钙的质量分数 某研究性学习小组设计了如下图所示的制气与除杂装置。请参与研究并回
为了粗略测定电石中碳化钙的质量分数,某研究性学习小组设计了如下图所示的制气与除杂装置。请参与研究并回答相关问题:(1)写出烧瓶B中发生反应的化学
(12分)某校化学兴趣小组学生为了探究乙酸 碳酸和苯酚的酸性强弱 该校学生先组装了右图的实验装置(夹
(12分)某校化学兴趣小组学生为了探究乙酸、碳酸和苯酚的酸性强弱,该校学生先组装了右图的实验装置(夹持仪器已略去)。进行了下述一些实验:(1)某生












