(1)图中所示反应是______(填“吸热”或“放热”)反应 该反应的△H=______(用含E1
| (1)图中所示反应是______(填“吸热”或“放热”)反应,该反应的△H=______(用含E1、E2的代数式表示). (2)已知热化学方程式:H2(g)+
(3)1L 1mol/L H2SO4溶液与2L 1mol/L NaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH反应的中和热的热化学方程式为______. (4)向1L1mol/L的NaOH溶液中加入:①浓H2SO4;②稀硝酸;③稀醋酸, 恰好完全反应的热效应△H1、△H2、△H3的大小关系为______. 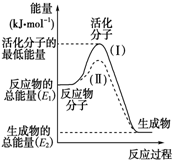 |
参考解答
| (1)依据图象分析反应物的能量大于生成物的能量,反应放热;反应的焓变=生成物的能量-反应物的能量,则△H=E2-E1, 故答案为:放热;E2-E1; (2)反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能+反应的焓变;H2(g)+
故答案为:409.0kJ/mol; (3)1L 1mol/L H2SO4溶液与2L 1mol/L NaOH溶液完全反应,放出114.6kJ的热量,则生成1mol水放出57.3kJ的热量,反应的热化学方程式为
故答案为:
(3)浓硫酸溶于水放热,醋酸为弱电解质,溶于水吸热,因反应热为负值,放出的热量越多,则△H越小,则△H3>△H2>△H1, 故答案为:△H3>△H2>△H1. |
相似问题
下列物质分别溶于水中 能使溶液温度显著升高的是
下列物质分别溶于水中,能使溶液温度显著升高的是()A.浓硫酸B.食盐C.酒精D.氯化铵
已知石墨和金刚石燃烧的热化学方程式如下:C(石墨 s)+O2(g) → CO2(g)+393.8 k
已知石墨和金刚石燃烧的热化学方程式如下:C(石墨,s)+O2(g) → CO2(g)+393 8 kJ ;C(金刚石,s)+O2(g) → CO2(g)+395 2 kJ下列说法中正确的
根据下图提供的信息 下列所得结论正确的是A.该反应是吸热反应B.该反应的生成物比反应物稳定C.该反应
根据下图提供的信息,下列所得结论正确的是A.该反应是吸热反应B.该反应的生成物比反应物稳定C.该反应一定可以设计成为原电池D.该反应向外界放出的热
(9分)“西气东输”是西部开发的重点工程 这里的“气”是指天然气 其主要成分是甲烷。水煤气中主要成分
(9分)“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。水煤气中主要成分是CO和H2,二者的体积比为l :l。已知:在120
(3分) 已知298K 101KPa时 1g液态甲醇(CH3OH)完全燃烧生成CO2和液态水 放出2
(3分) 已知298K、101KPa时,1g液态甲醇(CH3OH)完全燃烧生成CO2和液态水,放出22 5kJ的热量,请写出相应的热化学方程:。












