教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素 离子方程式为:2MnO4-+
教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(2)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4-)=______mol/L. (3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定______来比较化学反应速率. (4)小组同学发现反应速率总是如图二,其中t1~t2时间内速 率变快的主要原因可能是:①该反应放热、②______. 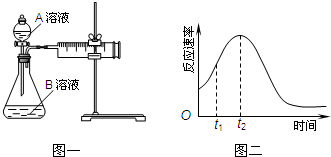 |
参考解答
| (1)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大,故答案为:浓度;②;①; (2)CO2的物质的量是:4.48mL×10-322.4mol/l=0.0002mol,设2min末,反应(MnO4-)为X 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 2 10 X 0.0002mol 解得 X=0.00004mol 30mL×10-3×0.01mol?L-1-0.00004mol=0.00026mol C(MnO4-)=nv=0.00026mol0.05L=0.0052mol/L 故答案为:0.0052; (3)通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率,故答案为:KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间; (4)催化剂能加快化学反应的速率,产物Mn2+(或MnSO4)是反应的催化剂,故答案为:产物Mn2+(或MnSO4)是反应的催化剂. |
相似问题
各可逆反应达平衡后 改变反应条件 其变化趋势正确的是( )A.B.C.D.
各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )A.B.C.D.
把4种不同体积 不同浓度的X溶液 分别加入4个盛有10mL 2mol?L-1盐酸的烧杯中 并加水稀释
把4种不同体积、不同浓度的X溶液,分别加入4个盛有10mL2mol?L-1盐酸的烧杯中,并加水稀释到50mL,此时X和盐酸进行反应,其中反应速率最大的是( )A.
盐酸与块状碳酸钙固体反应时 不能使反应的最初速率明显加快的是( )A.将块状碳酸钙固体换成粉末状固
盐酸与块状碳酸钙固体反应时,不能使反应的最初速率明显加快的是( )A.将块状碳酸钙固体换成粉末状固体B.盐酸的量增加一倍C.盐酸的用量减半浓度加
经研究知Cu2+对H2O2分解也具有催化作用 为比较Fe3+和Cu2+对H2O2分解的催化效果 某研
经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:(1)
下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体).请回答下列问题:(1
下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体).请回答下列问题:(1)能用作干燥氨气的装置有______(填字母);(












