某种牙膏中的摩擦剂是碳酸钙 可以用石灰石(含杂质SiO2)来制备.某同学甲设计了一种制备碳酸钙的方案
某种牙膏中的摩擦剂是碳酸钙,可以用石灰石(含杂质SiO2)来制备.某同学甲设计了一种制备碳酸钙的方案,其流程图为: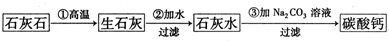 请回答下列问题: (1)假设第①步反应完全进行,则第②步反应过滤后得到的滤渣的成分为______. (2)第③步反应不使用CO2,其主要原因是(用离子方程式表示)______ ______. (3)第③步反应使用Na2CO3而不使用NaHCO3,从提高企业经济效益的角度考虑,其原因是______. (4)某同学乙用石灰石为原料(其他试剂自选),设计了另一种制备碳酸钙的实验方案,请你完成他的实验方案.  乙同学所设计的方案的优点是______. |
参考解答
| (1)石灰石(含杂质SiO2),依据流程图分析可知,石灰石高温分解生成氧化钙和二氧化碳,氧化钙和二氧化硅反应生成硅酸钙,溶于水氧化钙和水反应生成氢氧化钙,硅酸钙不溶,过滤得到硅酸钙,滤渣是CaSiO3; 故答案为:CaSiO3; (2)第③步反应不使用CO2,是因为二氧化碳和氢氧化钙反应生成碳酸钙,但二氧化碳过量会减小反应生成碳酸氢钙溶于水,反应的离子方程式为:Ca2+++CO2=CaCO3↓+H2O,CaCO3+CO2+H2O═Ca2++2HCO3-; 故答案为:Ca2+++CO2=CaCO3↓+H2O,CaCO3+CO2+H2O═Ca2++2HCO3-; (3)第③步反应使用Na2CO3而不使用NaHCO3,是因为生成等质量的CaCO3消耗NaHCO3多于Na2CO3,使用Na2CO3可制取副产品NaOH; 故答案为:生成等质量的CaCO3消耗NaHCO3多于Na2CO3;使用Na2CO3可制取副产品NaOH; (4)①利用碳酸钙和盐酸反应生成氯化钙溶液,在溶液中加入碳酸钠溶液生成碳酸钙沉淀,过滤得到固体, 故答案为:稀盐酸; CaCl2,Na2CO3; ②流程设计的优点是操作简单,无污染,节约原料; 故答案为:节约燃料,减小污染,操作简便; |
相似问题
断定NaHCO3白色粉末中是否混有Na2CO3的方法是( )A.加热观察是否有气体放出B.加盐酸并
断定NaHCO3白色粉末中是否混有Na2CO3的方法是( )A.加热观察是否有气体放出B.加盐酸并观察生成气体的速度C.Ba(OH)2溶液,观察有无白色沉淀生成D
化学实验室中常将溶液或试剂进行酸化 下列酸化处理中正确的是( )A.检验C2H5Cl中Cl元素时
化学实验室中常将溶液或试剂进行酸化,下列酸化处理中正确的是( )A.检验C2H5Cl中Cl元素时,将C2H5Cl和NaOH溶液混合加热后,加硫酸酸化B.鉴别溶液
下列有关物质分离 提纯方案正确的是( )A.除去铁粉中混有的I2:加热使I2升华B.除去NaCl固
下列有关物质分离、提纯方案正确的是( )A.除去铁粉中混有的I2:加热使I2升华B.除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶C.除
限用下列一种试剂鉴别氯化钠 氯化铝 氯化亚铁 氯化铁 氯化镁五种溶液 这种试剂是( )A.KSCN
限用下列一种试剂鉴别氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,这种试剂是( )A.KSCNB.HClC.BaCl2D.NaOH
下列各组物质 只用水不能加以区分的是( )A.溴蒸气 二氧化氮两种气体B.己烯 甲苯 四氯化碳三种
下列各组物质,只用水不能加以区分的是( )A.溴蒸气、二氧化氮两种气体B.己烯、甲苯、四氯化碳三种液体C.溴苯、苯、乙醛三种液体D.氯化钠、无水












