(4分)用石墨电极电解100 mLH2SO4和CuSO4的混合液 通电一段时间 两极上均产生2.24
| (4分)用石墨电极电解100 mLH2SO4和CuSO4的混合液,通电一段时间,两极上均产生2.24L(标准状况)气体,则原混合液中Cu2+的浓度是多少? |
参考解答
(4分)1mol/L 2CuSO4 +2H2O 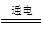 2Cu+O2↑+ 2H2SO4 2H2O 2Cu+O2↑+ 2H2SO4 2H2O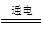 2H2↑ + O2↑ 写出电解总反应式给1分。 若用电子守恒法也对,给4分 2H2↑ + O2↑ 写出电解总反应式给1分。 若用电子守恒法也对,给4分n(H2)=n(O2)=0.1mol n(e-)总= 0.4mol n(e-)铜=' 0.4mol' - 2 n(H2)=0.2mol n(Cu) =' 0.1' mol C(Cu2+) =' 0.1mol/0.1L=1' mol/L |
| 考查电化学的有关计算。 通电一段时间,两极上均产生2.24L(标准状况)气体,所以电解时发生反应的方程式依次是2CuSO4 +2H2O 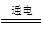 2Cu+O2↑+ 2H2SO4和2H2O 2Cu+O2↑+ 2H2SO4和2H2O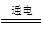 2H2↑ + O2↑。 2H2↑ + O2↑。由于n(H2)=n(O2)=2.24L÷22.4L/mol=0.1mol 所以转移电子是n(e-)总= 0.4mol 因此根据电子的得失守恒可知 n(e-)铜= 0.4mol - 2 n(H2)=0.2mol 所以n(Cu) =0.1 mol 因此c(Cu2+) = 0.1mol÷0.1L=1 mol/L |
相似问题
个别电解水设备推销商进行下列电解水实验:将纯净水与自来水进行对比 当电解器插入纯净水和自来水中通电数
个别电解水设备推销商进行下列电解水实验:将纯净水与自来水进行对比,当电解器插入纯净水和自来水中通电数分钟后,纯净水颜色无变化或略显黄色,而自来
用惰性电极电解稀HNO3 CuSO4和NaCl的混合液 最初一段时间阴极和阳极上分别析出的物质是A.
用惰性电极电解稀HNO3、CuSO4和NaCl的混合液,最初一段时间阴极和阳极上分别析出的物质是A.H2和Cl2B.Cu和Cl2C.H2和O2D.Cu和O2
如图所示装置中 a b都是惰性电极 通电一段时间后 b极附近溶液呈蓝色。下列说法中不正确的是(
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是()A.x是正极,y是负极B.x是负极,y是正极C.a极和Pt都
(8分)下图为以惰性电极进行电解。完成下列问题(1)A电极的现象是
(8分)下图为以惰性电极进行电解。完成下列问题(1)A电极的现象是B电极的电极反应方程式D电极的反应方程式(2)若电路中通过1mol电子,C电极的增重为g
将含有0.4molCu(NO3)2和0.4molKCl的水溶液1L用惰性电极电解一段时间后 在一个电
将含有0 4molCu(NO3)2和0 4molKCl的水溶液1L用惰性电极电解一段时间后,在一个电极上析出0 3molCu,此时在另一个电极上放出气体的体积(标准状况)约为(












