实验室采用MgCl2 AlCl3的混合溶液与过量氨水反应制备MgAl2O4 主要流程如下:(1)为使
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下: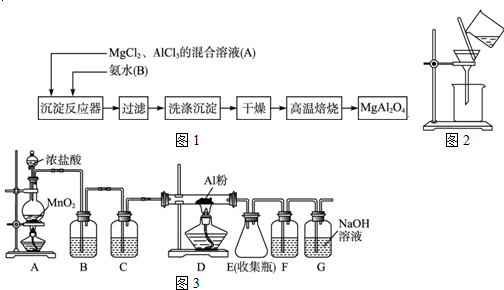 (1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入______(填“A”或“B”),再滴加另一反应物. (2)如下图所示,过滤操作中的一处错误是______. (3)判断流程中沉淀是否洗净所用的试剂是______.高温焙烧时,用于盛放固体的仪器名称是______. (4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备. 装置B中盛放饱和NaCl溶液,该装置的主要作用是______.F中试剂的作用是______.用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为______. |
参考解答
| (1)如先加入MgCl2、AlCl3的混合溶液,再加氨水,氨水少量,应先生成氢氧化镁沉淀,反之,先加氨水,因氨水足量,则同时生成沉淀,故答案为:B; (2)过滤时应该将漏斗的尖嘴部分紧贴烧杯的内壁,防止液体溅出,故答案为:漏斗下端尖嘴未紧贴烧杯内壁; (3)沉淀中应该附着氯离子和铵根离子,若判断是否洗净,可以取少量最后一次洗涤液,加入AgNO3溶液(或硝酸酸性的AgNO3溶液)溶液进行判断,若生成白色沉淀,则说明没有洗涤干净;若没有沉淀生成,则说明已经洗涤干净,高温焙烧固体应在坩埚中进行, 故答案为:AgNO3溶液(或硝酸酸性的AgNO3溶液);坩埚; (4)B中的饱和食盐水是为了除去混有的HCl气体;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以可以加入碱石灰来代替F和G的作用, 故答案为:除去HCl;吸收水蒸气;碱石灰. |
相似问题
下列根据实验现象所得出的结论中 一定正确的是( )A.无色试液使蓝色石蕊试纸变红 结论:溶液显碱性
下列根据实验现象所得出的结论中,一定正确的是( )A.无色试液使蓝色石蕊试纸变红,结论:溶液显碱性B.无色溶液焰色反应呈黄色,结论:试液是钠盐
为使人们确知含碘物质的存在 研究性学习小组同学设计了一种简便的检验方法 利用该物质在酸性条件下与KI
为使人们确知含碘物质的存在,研究性学习小组同学设计了一种简便的检验方法,利用该物质在酸性条件下与KI反应有单质碘生成的性质,选用下列生活常见的物
下列实验能达到预期目的是( )A.实验内容:向甲酸和甲醛的混合物中加入氢氧化钠溶液 中和甲酸后 加
下列实验能达到预期目的是( )A.实验内容:向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热实验目的:检验混合物中是
下列有关物质分离方法的叙述中 不正确的是( )A.用过滤的方法分离溶液和胶体B.用蒸馏的方法将自来
下列有关物质分离方法的叙述中,不正确的是( )A.用过滤的方法分离溶液和胶体B.用蒸馏的方法将自来水制成蒸馏水C.用四氯化碳萃取碘水中的碘D.用
要证明某溶液中不含Fe3+而可能含有Fe2+.进行如下实验操作时最佳顺序为( ) ①加入足量氯水
要证明某溶液中不含Fe3+而可能含有Fe2+.进行如下实验操作时最佳顺序为( )①加入足量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液.A.③①B.③②












