(1)控制变量是科学研究中的重要研究方法 其基本思路是 在实验研究中人为只改变一个因素(调节变量)
| (1)控制变量是科学研究中的重要研究方法,其基本思路是,在实验研究中人为只改变一个因素(调节变量),其他因素保持相同,观察测定因调节变量改变而改变的因素(因变量),从而分析得到研究结论.中学化学中应用控制变量的方法研究问题的例子很多.请分析或设计: ①在研究浓度对化学反应速率的影响时,教材安排了利用Na2S2O3与H2SO4反应的一组对照实验(Na2S2O3+H2SO4 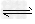 Na2SO4+S↓+SO2↑+H2O) 为0.20 mol/L, c(OH-)的起始浓度为1.50 mol/L,则反应速率v=____________. Na2SO4+S↓+SO2↑+H2O) 为0.20 mol/L, c(OH-)的起始浓度为1.50 mol/L,则反应速率v=____________. |
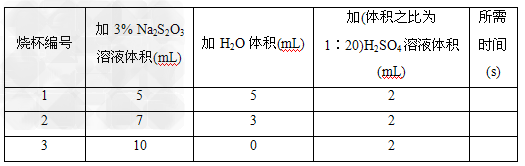 |
| 在三个烧杯(底部有黑色“十”字标记)内分别加入表中所示体积的三种液体,搅拌并开始计时,到出现浑浊使烧杯底部“十”字看不见时停止计时.比较所需时间,得出浓度对化学反应速率影响的结论.实验中,温度和反应体系中硫酸浓度是保持相同的因素,调节变量是________,因变量是________. ②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:___________________________________________________. (2)373 K时,H2PO3-与OH-发生如下反应: H2PO3-+OH- 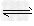 HPO32-+H2O 反应结果如下表所示: HPO32-+H2O 反应结果如下表所示: |
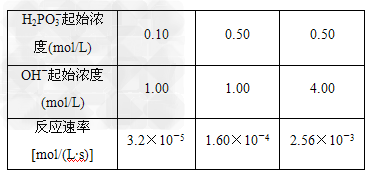 |
| 如果用v=kcm(H2PO3-)·cn(OH-)表示反应速率(k为与浓度无关的常数) ①k=________, m=________, n=________. ②若c(H2PO4-)的起始浓度为0.20 mol/L, c(OH-)的起始浓度为1.50 mol/L,则反应速率v=____________. |
参考解答
| (1)①Na2S2O3溶液的浓度 ;所需时间 ②取三支试管各放同浓度同体积的纯碱溶液,滴1~2滴酚酞试液,第一支不加热,第二支加热至t1℃,第三支加热至t2℃,观察三支试管中溶液的颜色深浅,温度越高,颜色越深,说明碱性越强,则水解程度越大(其他合理答案均给分,例如不同温度下测定同浓度同体积纯碱溶液的pH) (2)①3.2×10-4 ;1 ;2 ②1.44×10-4mol/(L·s) |
相似问题
为探究一溴环己烷()与NaOH的醇溶液共热发生的是水解反应还是消去反应 甲 乙 丙三位同学分别设计如
为探究一溴环己烷()与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:甲:向反应混合液中滴入稀硝酸中和N
某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC-COOH 可简写为H2C2O4)俗称
某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,
氧化铜有多种用途 如作玻璃着色剂 油类脱硫剂等 为获得纯净的氧化铜以探究其性质 某同学用工业硫酸铜(
氧化铜有多种用途,如作玻璃着色剂,油类脱硫剂等,为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:(1)制备氧
新型材料纳米α-Fe粉具有超强的磁性能 可用作高密度磁记录的介质以及高效催化剂等。在不同温度下 α-
新型材料纳米α-Fe粉具有超强的磁性能,可用作高密度磁记录的介质以及高效催化剂等。在不同温度下,α-Fe粉与蒸气反应的固体产物不同:温度低于570℃时,
用如图所示装置进行实验 将A逐滴加入B中。(1)若A为浓硫酸 B为第三周期金属元素的片状单质 其在常
用如图所示装置进行实验,将A逐滴加入B中。(1)若A为浓硫酸,B为第三周期金属元素的片状单质,其在常温下难与水反应;C为品红溶液,实验中观察到C中溶液












