实验室里需要纯净的氯化钠晶体 但现在只有混有硫酸钠 碳酸氢铵的氯化钠.某学生设计了如下方案:请回答下
实验室里需要纯净的氯化钠晶体,但现在只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案: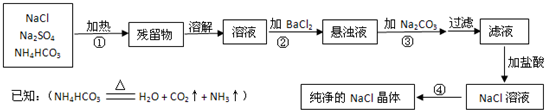 请回答下列问题: (1)操作①加热的目的是______,发生的反应______(填“是”或“不是”)氧化还原反应. (2)操作②除用BaCl2溶液外,还可以用______. (3)操作③的目的是______,发生反应的离子方程式为:______. (4)操作④应在______(填仪器名称)中进行. |
参考解答
| (1)操作①加热的目的是利用碳酸氢铵受热分解生成氨气、二氧化碳、水蒸气除去碳酸氢铵固体;发生的是碳酸氢铵分解的反应,反应前后无元素化合价变化,不是氧化还原反应,故答案为:除去混合物中的碳酸氢铵;不是; (2)操作②是完全沉淀硫酸根离子,原则是加入的试剂不能引入新的杂质,或最后易于除去,除了用BaCl2溶液外,也可以用Ba(OH)2溶液,故答案为:Ba(OH)2溶液; (3)操作③是加入碳酸钠溶液,目的是除去过量的钡离子,避免引入钡离子杂质,所以加入碳酸钠的目的是除去过量的Ba2+,反应的离子方程式为:Ba2++CO32-=BaCO3↓, 故答案为:除去过量的钡离子;Ba2++CO32-=BaCO3↓; (4)操作④是对饱和食盐水蒸发溶剂得到溶质晶体,溶液蒸发应在蒸发皿中加热进行,故答案为:蒸发皿. |
相似问题
现有某一含2mol/L的Mg2+ 2mol/L的Al3+的氯化镁和氯化铝溶液200ml.(1)该溶液
现有某一含2mol L的Mg2+、2mol L的Al3+的氯化镁和氯化铝溶液200ml.(1)该溶液中Cl-物质的量浓度是______;要将溶液中Mg2+转化为沉淀完全分离,至少需加
在粗盐提纯的实验中 每一步中玻璃棒的作用分别是(填序号)A.引流 B.搅拌 加速固体溶解 C.转移固
在粗盐提纯的实验中,每一步中玻璃棒的作用分别是(填序号)A.引流 B.搅拌,加速固体溶解 C.转移固体 D.搅拌,防止液滴飞溅 溶解__________过滤_
实验室需用480mL0.2mol?L-1的稀硫酸 现用18.4mol?L-1的浓硫酸来配置.(1)计
实验室需用480mL0 2mol?L-1的稀硫酸,现用18 4mol?L-1的浓硫酸来配置.(1)计算所需浓硫酸的体积为______mL.(2)所需仪器除了玻璃棒、烧杯、胶头滴管
为除去粗盐中的CaCl2 MgCl2 FeCl3 Na2SO4以及泥沙等杂质 某同学设计了一种制备精
为除去粗盐中的CaCl2、MgCl2、FeCl3、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):(1)第①步操作
某研究性学习小组对粗盐的提纯和检验进行研究 他们查得有关资料如下表所示。 【有关资料】 【设计除杂过
某研究性学习小组对粗盐的提纯和检验进行研究,他们查得有关资料如下表所示。 【有关资料】 【设计除杂过程】 已知该粗盐样品中主要含有不溶性杂质、M












