二氧化钛(TiO2)广泛用于制造高级白色油漆 也是许多反应的催化剂.工业上用钛铁矿[主要成分为FeT
二氧化钛(TiO2)广泛用于制造高级白色油漆,也是许多反应的催化剂.工业上用钛铁矿[主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2杂质]作原料,制取二氧化钛及绿矾,其生产流程如下: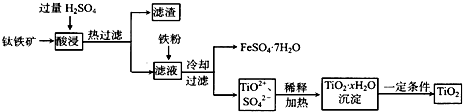 回答下列问题: (1)Ti原子序数为22,则Ti位于周期表第______周期,第______列. (2)FeTiO3溶于过量硫酸的离子方程式______. (3)流程中生成TiO2?xH2O离子方程式为______. (4)若铁粉的用量不足,可能导致产品TiO2中混有______杂质. (5)以TiO2为原料制取金属钛的其中一步反应为TiO2+Cl2+C
(6)TiCl4 在常温下呈液态,且极易水解,可以用作军事烟雾剂;写出其水解反应的方程式______. |
参考解答
| (1)22-2-8-8=4,故Ti元素处于第四周期,第4列. 故答案为:四、4. (2)由工艺流程转化关系可知,FeTiO3溶于过量硫酸,生成Fe2+、TiO2+、H2O,反应离子方程式为FeTiO3+4H+=Fe2++TiO2++2H2O. 故答案为:FeTiO3+4H+=Fe2++TiO2++2H2O. (3)由工艺流程转化关系可知,TiO2+在加热条件下与水反应生成TiO2?xH2O,根据电荷守恒可知还生成H+,所以反应离子方程式为TiO2++(x+1)H2O=TiO2?xH2O+2H+. 故答案为:TiO2++(x+1)H2O=TiO2?xH2O+2H+. (4)铁粉的用量不足,滤液中的Fe3+,不能除尽.生成的TiO2?xH2O沉淀中含有氢氧化铁,最后氢氧化铁分解生成氧化铁,所以可能导致产品TiO2中混有Fe2O3. 故答案为:Fe2O3. (5)反应中Ti元素化合价未变化,氯元素化合价由0价降低为-1价,令碳元素在产物中等化合价为a,则a=2×[0-(-1),故a=2,反应中氧化剂与还原剂的物质的量之比为1:1,结合元素守恒可知,TiO2、Cl2、C、TiCl4的系数分别为1、2、2、1,所以未知物中含有C原子与O原子,碳元素化合价为+2,故为CO,系数为2. 故答案为:2CO;CO. (6)TiCl4 水解,生成H2TiO3与HCl,H2TiO3是固体颗粒,HCl与空气中水蒸气结合呈白雾,可以用作军事烟雾剂.水解方程式为TiCl4?+3H2O=H2TiO3+3HCl↑. 故答案为:TiCl4?+3H2O=H2TiO3+3HCl↑. |
相似问题
下列各组物质中 仅用水及物质间相互反应不能一一区别的一组是( )A.Na2O2 Al2(SO4)3
下列各组物质中,仅用水及物质间相互反应不能一一区别的一组是( )A.Na2O2 Al2(SO4)3 MgCl2 K2CO3B.BaCl2 Na2SO4 (NH4)SO4 KOHC.AgNO3
某化学兴趣小组欲研究FeCl3.稀H2SO4.KCl.NaCl.Na2CO3.NaOH的性质 对于如
某化学兴趣小组欲研究FeCl3.稀H2SO4.KCl.NaCl.Na2CO3.NaOH的性质,对于如何研究,他们设计了两种研究方案:方案①:将它们按照酸.碱.盐分类,然后
如图所示装置进行实验(图中铁架台等仪器均已略去).在I中加入试剂后 塞紧橡皮塞 立即打开止水夹 II
如图所示装置进行实验(图中铁架台等仪器均已略去).在I中加入试剂后,塞紧橡皮塞,立即打开止水夹,II中有气泡冒出;一段时间后关闭止水夹,II中液面上
下列各组气体或溶液用括号内试剂加以鉴别 其中合理的是( )A.氯化铵 硫酸铵 碳酸铵(氢氧化钡溶液
下列各组气体或溶液用括号内试剂加以鉴别,其中合理的是( )A.氯化铵、硫酸铵、碳酸铵(氢氧化钡溶液)B.氯化钠、硫酸钠、碳酸钠(硝酸银溶液、稀
有四瓶常用溶液:①BaCl2溶液 ②NaCl溶液 ③Na2SO4溶液 ④CuSO4溶液.不用其他试剂
有四瓶常用溶液:①BaCl2溶液②NaCl溶液③Na2SO4溶液④CuSO4溶液.不用其他试剂,可通过实验方法将它们一一鉴别出来,被鉴别的先后顺序是( )A.①④












