高温下 某反应达到平衡 平衡常数。恒容时 温度升高 H2浓度减小。下列说法正确的是[ ]A.
高温下,某反应达到平衡,平衡常数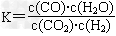 。恒容时,温度升高, 。恒容时,温度升高,H2浓度减小。下列说法正确的是 |
| [ ] |
| A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小 C.升高温度,逆反应速率减小 D.该反应的化学方程式为CO+H2O  CO2+H2 CO2+H2 |
参考解答
| A |
相似问题
25℃时 在含有Pb2+ Sn2+的某溶液中 加入过量金属锡(Sn) 发生反应:Sn(s)+Pb2+
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。 下
某温度下 在一容积可变的容器中 反应2A(g)+B(g) 2C(g)达到平衡时 A B和C的物质的量
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2 mol和4 mol。保持温度和压强不变,对平衡
.超音速飞机在平流层飞行时 尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO22CO2 +N2。为了测
在一密闭容器中发生反应:L(s)+aG(g)bR(g) 下图是温度和压强对该反应的影响 其中压强P1
在一密闭容器中发生反应:L(s)+aG(g)bR(g) 下图是温度和压强对该反应的影响,其中压强P1<P2,由此可以判断 [ ]A.正反应为放热反应 B.化学方程式中
将装有1mol NH3的密闭容器加热 部分NH3分解后达到平衡 此时混合气中NH3的体积分数为x%;
将装有1mol NH3的密闭容器加热,部分NH3分解后达到平衡,此时混合气中NH3的体积分数为x%;若在同一容器中最初加入的是2mol NH3,密封、加热到相同温度












