某校研究性学习小组拟利用分光光度法对空气中二氧化硫含量(mg/m3)进行测定。分光光度法则是通过测定
某校研究性学习小组拟利用分光光度法对空气中二氧化硫含量(mg/m3)进行测定。分光光度法则是通过测定被测物质在特定波长时光的吸收度,对该物质进行定性和定量分析。其工作原理可以简单的用公式表示为A=kc,其中A为吸光度,k为一定条件下的常数,c为溶液浓度。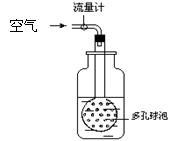  实验步骤如下: ⑴ 采样: ① 如果你是该小组成员,你对采样的地点和时间有何建议: 。 ② 用右图装置采样,通过50L空气后,将吸收液移入100ml容量瓶,用少量吸 收液分两次洗涤吸收装置,合并洗涤液于容量瓶中,定容备用。用多孔球泡而不 用导管的原因是 。 ⑵ 吸光度与SO2含量标准曲线的绘制:在6支25ml比色管中,用每毫升含25μg 二氧化硫的标准液配置下表标准SO2含量系列。 二氧化硫标准系列
⑶ 准确量取容量瓶中溶液10mL加入比色皿,测得其吸光度值 为0.10,则空气中二氧化硫含量为 mg/m3。我国环境空气 质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3): 一级标准:0.15;二级标准:0.50;三级标准:0.70。 则该市空气为 级标准。 ⑷ 甲、乙两组同学测定结果相差较大,乙组同学测定空气中SO2 含量偏小,试分析乙组同学出现误差的可能原因: (两个所用 药品和装置均无问题)。 |
参考解答
⑴ ① 在不同地点、不同时间采样,如学校、工厂、居民区附近;早晨、中午、晚上分别采样 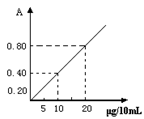 ② 使二氧化硫能被吸收液充分吸收 ⑵ (见右图) ⑶ 0.5 二级标准 ⑷ 抽气速率过快,造成空气中SO2与吸收液未充分反应,产生较大误差 |
| B.本题考查化学实验。(1)①时间与地点的不同,可以提高测定数据的准确性。②多孔球泡的表面积比导管与溶液的接触面积要大得多,这样吸收更充分。(2)结合表中数据,找出关键点,如10.00ml对应的A为0.4,20.00ml对应的A为0.8,其他采用描点,即可作出标准线。(3)表格中的比例关系知,吸光度为0.1时,二氧化硫的含为2.5μg/ 10mL= 25ug/100mL,而空气为50L,则空气中二氧化硫含量为:25ug/50L='0.5' mg/m3,则对应为二级标准。(4)SO2含量偏小,其原因应为SO2的反应不充分,没有全部吸收。 |
相似问题
某兴趣小组对如何延长硫酸亚铁溶液的保质期展开了研究。(1)制备硫酸亚铁溶液 最合适的试剂组为____
某兴趣小组对如何延长硫酸亚铁溶液的保质期展开了研究。(1)制备硫酸亚铁溶液,最合适的试剂组为___________(填编号); a.过量铁屑和稀硫酸b.过量
在酸性条件下H2C2O4可以被KMnO4溶液氧化 使KMnO4溶液褪色 依据KMnO4溶液褪色时间的
在酸性条件下H2C2O4可以被KMnO4溶液氧化,使KMnO4溶液褪色,依据KMnO4溶液褪色时间的长短可以比较反应进行的快慢。下列各组实验中溶液褪色最快的是组号反
(15分)甲 乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀 用下图所示装置进
(15分)甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)实验
有A B C三瓶失去标签的无色溶液:K2CO3 BaCl2 NaSO4。将它们分别与H2SO4作用
有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、NaSO4。将它们分别与H2SO4作用,A产生白色沉淀,B产生无色气体,C中无明显现象。则A是________,B是________, C是________。
某课外兴趣小组在进行“诚信商品”实验时 随机抽取市售“碳酸氢钠”样品(成分说明见右表所示)。经检验杂
某课外兴趣小组在进行“诚信商品”实验时,随机抽取市售“碳酸氢钠”样品(成分说明见右表所示)。经检验杂质只含NaCl,准确称取8 5g样品,加入100mL盐酸












