某校研究性学习小组选择使用下列仪器和药品 验证铜和适量浓硝酸反应除生成NO2外 还生成少量的NO(实
| 某校研究性学习小组选择使用下列仪器和药品,验证铜和适量浓硝酸反应除生成NO2外,还生成少量的NO(实验中使用的N2和O2的用量可自由控制)。已知: ①NO+NO2+2OH-=2NO2- +H2O ②气体液化温度: NO2 21℃ NO -152℃ 请回答: |
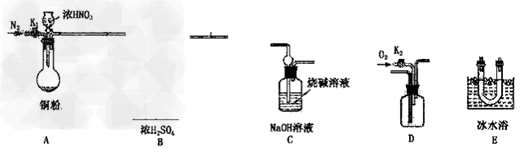 |
| (1)写出铜与浓硝酸反应的化学反应方程式___________。 (2)装置B的作用是___________,在上图方框内画出B装置。 (3)写出装置的连接顺序(填字母):A接B接_____________。 (4)实验开始前要先打开A装置中的活塞K1,持续通一段时问氮气后再关闭活塞K1,目的是___________ 。A中的反应停止后,打开D中的活塞K2,并通人氧气,若反应中确有NO产生,则D中出现的现象是______________。 (5)如果O2过量,则装置C中发生反应的离子方程式是____________。 (6)若铜粉中混入了少量的Ag,已知铜粉质量为a g,反应后固体完全溶解,要测定铜粉中铜的质量分数,只需利用A装置中反应后的溶液进行简单的实验操作,就可以达到实验目的。试简述实验方案_______________。 |
参考解答
| (1)Cu +4HNO3(浓) = Cu(NO3)2 + 2NO2 ↑ +2 H2O (2)吸收水蒸汽,防止在E中与NO2反应生成NO ;  (3)EDC (4)排除装置中的空气,防止与生成的NO反应;出现红棕色气体 (5)4NO2+O2+4OH-=4NO3-+2H2O (6)在A的溶液中加入过量的氯化钠,过滤,洗涤、干燥沉淀,再称质量。 |
相似问题
下列实验方案设计正确的是[ ]A.分解高锰酸钾制取氧气后 残留在试管内壁上的黑色物质可用稀盐
下列实验方案设计正确的是[ ]A.分解高锰酸钾制取氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 B.失去标签的AgNO3溶液、稀盐酸、NaOH溶液、AlCl
某学习小组通过测定大理石与硝酸反应过程中体系质量的变化 研究影响反应速率的因素。所用HNO3浓度为1
某学习小组通过测定大理石与硝酸反应过程中体系质量的变化,研究影响反应速率的因素。所用HNO3浓度为1 00 mol L、2 00 mol L,大理石有细颗粒与粗颗粒
甲 乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀 用下图所示装置进行实验(夹
甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。 实验操作
为探究乙烯与溴的加成反应 甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2O
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2OHCH2=CH2↑+H2O),将生成的气体直接通入溴水中,发现溶
在常温下 Fe与水并不起反应 但在高温下 Fe与水蒸气可发生反应。 应用下列装置 在硬质玻璃管中放入
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就












