(12分)2SO2(g)+ O2(g) 2SO3(g) △H =- a kJ·mol-1 反应过程的
(12分)2SO2(g)+ O2(g) 2SO3(g) △H =- a kJ·mol-1,反应过程的能量变化如图所示。已知1mol SO2(g)完全转化为1mol SO3(g)放热99 kJ。请回答: 2SO3(g) △H =- a kJ·mol-1,反应过程的能量变化如图所示。已知1mol SO2(g)完全转化为1mol SO3(g)放热99 kJ。请回答: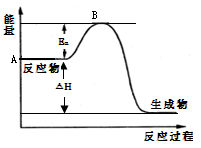 ⑴图中A点表示__________________,a=__________。 ⑵Ea的大小对该反应的△H _______(填“有”或“无”)影响。该反应常用V2O5作催化剂,加入V2O5会使图中B点_________(填“升高”、“降低”或“不变”)。 ⑶已知单质硫的燃烧热为296kJ·mol-1,写出反应的热化学方程式:_____________________,常温常压下,由单质硫和氧气经两步反应,生成3 mol SO3(g),放出的总热量为___ _。 |
参考解答
| (12分)⑴反应物的总能量 198 ⑵无 降低 ⑶S(s)+ O2(g)=SO2(g)△H=-296 kJ·mol-1 1185 kJ |
试题分析:(1)根据图像可知,A点表示反应物的总能量。1mol SO2(g)完全转化为1mol SO3(g)放热99 kJ,所以a=99×1=198。 (2)Ea表示活化能,其大小对该反应的△H无影响。催化剂能降低反应的活化能,从而加快反应速率。 (3)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以根据单质硫的燃烧热为296kJ·mol-1可知,该反应的热化学方程式是S(s)+ O2(g)=SO2(g)△H=-296 kJ·mol-1。根据盖斯定律可知,S直接生成SO3的热化学方程式是S(s)+ 3/2O2(g)=SO3(g)△H=-395 kJ·mol-1,所以生成3 mol SO3(g),放出的总热量为3mol×395kJ/mol=1185kJ。 点评:在计算反应热时,常常需要根据盖斯定律并结合数学知识进行。需要注意的是,在扩大化学计量数时,不要忘记了反应热也要同步扩大相应的倍数。 |
相似问题
(15分)下列物质①铁 ②干冰 ③金刚石 ④铜 ⑤水晶 ⑥氯化钠 ⑦单质碘⑧氢氧化钠【请用编号回答(
(15分)下列物质①铁②干冰③金刚石④铜⑤水晶⑥氯化钠⑦单质碘⑧氢氧化钠【请用编号回答(1)和(2)小题】(1)属于离子晶体的是,属于分子晶体的是,
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ 且1mol O2的化学键完全断裂时吸收热量496
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且1mol O2的化学键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则氢气中1mol H
能说明苯分子中碳碳键不是单 双键相间交替的事实是①苯不能使酸性KMnO4溶液褪色 ②苯环中碳碳
能说明苯分子中碳碳键不是单、双键相间交替的事实是①苯不能使酸性KMnO4溶液褪色②苯环中碳碳键均相同③邻二甲苯只有一种④苯的对位二元取代物只有一种⑤
请判断在下列物理变化过程中 化学键被破坏的是 A.碘升华B.溴蒸气被木炭吸附C.葡萄糖在水中的扩散D
请判断在下列物理变化过程中,化学键被破坏的是 A.碘升华B.溴蒸气被木炭吸附C.葡萄糖在水中的扩散D.氯化钠晶体溶于水
下列物质中只含共价键的是A.H2OB.Na2O C.CaCl2D.NH4Cl
下列物质中只含共价键的是A.H2OB.Na2O C.CaCl2D.NH4Cl












