A B C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。 (1)A中反应的离子方程式为________
| A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。 |
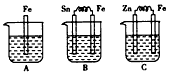 |
| (1)A中反应的离子方程式为_____________________。 (2)B中Sn极的电极反应式为_____________________。 (3)C中被腐蚀的金属是____,总反应方程式为_____________________ 。比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________。 |
参考解答
| (1)Fe+2H+ = Fe2++H2↑ (2)2H++2e- = H2 ↑ (3)Zn;Zn+H2SO4 = ZnSO4+H2↑ |
相似问题
下列关于实验现象的描述不正确的是 [ ]A.把铜片和铁片紧靠在一起浸入稀硫酸中 铜片表面出现
下列关于实验现象的描述不正确的是 [ ]A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 B.把铁片插入硫酸铜溶液中,铁片表面附着一层紫红
下列有关电化学知识的描述正确的是 [ ]A.CaO+H2O== Ca(OH)2 可以放出大量
下列有关电化学知识的描述正确的是 [ ]A.CaO+H2O== Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 B.某原电池
碱性电池具有容量大 放电电流大的特点 因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液 电池总
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+
铁及铁的化合物应用广泛 如FeCl3可用作催化剂 印刷电路铜板腐蚀剂和外伤止血剂等。 (1)写出Fe
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。 (1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:______________
正极材料为的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。(1)橄榄石型是一种
正极材料为的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。(1)橄榄石型是一种潜在的锂离子电池正极材料,它可以通过、与溶液












