氮气是制备含氮化合物的一种重要物质 而氮的化合物用途广泛。 (1)下面是氮气的一种利用途径: 过程Ⅱ
| 氮气是制备含氮化合物的一种重要物质,而氮的化合物用途广泛。 (1)下面是氮气的一种利用途径: |
 |
| 过程Ⅱ的化学方程式是____ 。 (2)氨气的制备与运输过程中都有严格要求。 ①合成氨时,温度过高,氨气的产率降低,试从化学平衡移动原理的角度加以解释:____ 。 ②运输时,严禁与卤素(如Cl2)混装运输。二者接触时会剧烈反应产生白烟,且0.4 mol NH3参加反应时有 0.3 mol电子转移。写出反应的化学方程式:___。 ③工业上可用碱性溶液通过电解的方法实现由N2制取NH3:2N2+6H2O  4NH3+3O2,通入N2的一极是___ (填“阴极”或“阳极”),阳极的电极反应式是____。 4NH3+3O2,通入N2的一极是___ (填“阴极”或“阳极”),阳极的电极反应式是____。 (3)已知:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1 316 kJ.mol-1 氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。 ①能利用该反应设计成电池的原因是___。 ②燃料电池的负极反应式是___。 |
参考解答
(l)N2 +3H2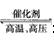 2NH3 (或 N2 +O2 2NH3 (或 N2 +O2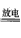 2NO) 2NO) (2)①合成氨的反应是一个放热反应,升高温度,平衡向生成氮气和氢气的方向移动,从而使氨气的产率降低 ; ②8NH3 +3Cl2==6NH4Cl+N2 ; ③阴极;4OH--4e-==O2↑+2H2O (3)①该反应为自发的、放热的氧化还原反应 ;②2NH3 -6e-+6OH-==N2↑+6H2O |
相似问题
锂电池是一代新型高能电池 它以质量轻 能量高而受到了普遍重视 目前已研制成功多种锂电池。某种锂电池的
锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应式为Li+MnO2=LiMnO2,下列说法正确的是
依据氧化还原反应:2Ag+(aq)+ Cu(s)===Cu2+(aq) +2Ag(s)设计的原电池如
依据氧化还原反应:2Ag+(aq)+ Cu(s)===Cu2+(aq) +2Ag(s)设计的原电池如图所示。 请回答下列问题: (1)电极X的材料是____;电解质溶液Y是____; (
下列叙述中不正确的是[ ]A.金属的电化腐蚀比化学腐蚀普遍B.钢铁在干燥空气里不易腐蚀 C.
下列叙述中不正确的是[ ]A.金属的电化腐蚀比化学腐蚀普遍B.钢铁在干燥空气里不易腐蚀 C.用铝质铆钉铆接铁板,铁板易被腐蚀 D.原电池中电子由正极流入负极
下图装置中 U型管内为红墨水 a b试管内分别盛有食盐水和氯化铵溶液 各加入生铁块 放置一段时间。下
下图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是 [ ]A.生铁块中的碳是原电
用铜片 银片 Cu(NO3)2溶液 AgNO3溶液 导线和盐桥(装有琼脂-KNO3的U型管)构成一个
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是[ ]①在外电路中,电流由












