有A B两个起始容积相等的恒温密闭容器 A保持恒压 B保持恒容.起始时向A B中均通入2molSO2
| 有A、B两个起始容积相等的恒温密闭容器,A保持恒压,B保持恒容.起始时向A、B中均通入2molSO2和1molO2后,在一定条件下反应达到平衡.则下列说法中不正确的是 A.达到平衡时,SO2的转化率:A<B B.起始时的反应速率:A=B,反应完成时的平均速率:A<B C.达到平衡后再充入等量氦气,A、B中平衡均不发生移动 D.若再向A中充入2molSO3,平衡时SO2的质量分数不变 |
参考解答
| BCD |
2SO2+O2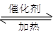 2SO3属于正反应气体系数减小的可逆反应,反应进行时气体的总物质的量减小,A容器恒压,容器内气体的压强不变,而B容器恒容,容器内气体的压强减小,故A相对于B来说,相当于加压 2SO3属于正反应气体系数减小的可逆反应,反应进行时气体的总物质的量减小,A容器恒压,容器内气体的压强不变,而B容器恒容,容器内气体的压强减小,故A相对于B来说,相当于加压A:加压,平衡正向移动,SO2的转化率增大,故A>B,不正确 B:起始时两容器反应状态完全相同,反应速率相等,反应完成时,A容器内压强大,反应速率快,即A>B,不正确 C:达到平衡后再充入等量氦气,A容器相当于减压,平衡左移,而B容器内各物质的浓度不变,正逆反应速率仍旧相等,平衡不移动,不正确 D:在恒压情况下,若再向A中充入2molSO3,与原平衡等效,平衡时SO2的质量分数不变,正确 故答案为BCD |
相似问题
(12分)化学平衡原理在工农业生产中发挥着重要的指导作用。(1)反应C(s)+CO2(g) 2CO(
(12分)化学平衡原理在工农业生产中发挥着重要的指导作用。(1)反应C(s)+CO2(g) 2CO(g)平衡常数K的表达式为;已知C(s) + H2O(g)CO(g)+H2(g)的平衡常数为
(4分)一定条件下的可逆反应2NO2 (g) ≒ N2O4 (g) △H= -92.4kJ/mol达
(4分)一定条件下的可逆反应2NO2 (g) ≒ N2O4 (g) △H= -92 4kJ mol达到化学平衡状态且其它条件不变时,(1)如果升高温度,平衡混合物的颜色;(
(12分)已知下列反应:① N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ·mo
(12分)已知下列反应:①N2(g)+3H2(g) 2NH3(g);ΔH=-92 4 kJ·mol-1。② 4NH3(g)+5O2(g)=====4NO(g)+6H2O(g);ΔH<0(1)在500℃、2 02×107Pa和
体积相同的甲和乙两个容器中 分别都充有等物质的量的SO2和O2 在相同温度下发生反应:2SO2+O2
体积相同的甲和乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 2SO3,并达到平衡,在该过程中,甲容器保持体积不变,乙容器保持
一定温度下 在密闭容器中可逆反应.N2(g)+3H2(g)2NH3(g)达到平衡状态 此时N2的转化
一定温度下,在密闭容器中可逆反应.N2(g)+3H2(g)2NH3(g)达到平衡状态,此时N2的转化率为20%,H2的转化率为50%,则平衡时体系的压强为反应前的()












