如图装置中 A B中电极为多孔的惰性电极;C D为夹在湿的Na2SO4滤纸条上的铂夹 a b为电源两
如图装置中,A、B中电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹,a、b为电源两极.在A、B中充满KOH溶液后使其倒立于盛有KOH溶液的水槽中.切断K1,闭合K2、K3,通直流电,电解一段时间后A、B中产生体积不相等的无色气体,如图所示. 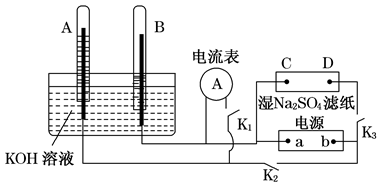 (1)试管B中收集的气体是 (填化学式)电源的a极为 (填“正极”或“负极”). (2)写出铂夹C上发生的电极反应式: (3)写出A中电极反应式: . (4)若电解一段时间后A、B中均有气体包围电极.此时切断K2、K3,闭合K1,电流表的指针发生偏转,此时B极的电极反应式为 . |
参考解答
| (1)H2 负极 (2)2H+ + 2e- = H2↑ (3)4OH- - 4e- = O2↑+2H2O (4)H2+2OH- -2e- = 2H2O |
①切断K1,合闭K2、K3通直流电,电极A、B及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为2:1,通过图象知,B极上气体体积是A极上气体体积的2倍,所以B极上得氢气,A极上得到氧气,所以B极是阴极,A极是阳极,故a是负极,b是正极. 故答案为:B极上得氢气,负; ⑵C极上氢离子得电子生成氢气,电极反应式为4H++4e=2H2↑. 故答案为: 4H++4e=2H2↑; ⑶A极上氢氧根离子失电子生成氧气和水,电极反应式为4OH--4e=2H2O+O2↑; 故答案为:4OH--4e=2H2O+O2↑; ⑷切断K2、K3,合闭K1,电解一段时间后,A、B中均有气体包围电极.此装置构成氢氧燃料原电池,所以有电流通过,电流表的指针移动.此时B极为负极,电极反应式为H2+2OH- -2e- = 2H2O 故答案为:H2+2OH- -2e- = 2H2O |
相似问题
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O 研读图 下列判断不正确的
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是( )A.K闭合时,d电极反应式:PbSO4+2H2O-2e-═PbO2+4H++SO42-B.
将纯锌片和纯铜片按图所示插入相同浓度的稀硫酸中 以下有关叙述正确的是A.甲装置子中电能转化为化学能B
将纯锌片和纯铜片按图所示插入相同浓度的稀硫酸中,以下有关叙述正确的是A.甲装置子中电能转化为化学能B.乙装置中电能转化为化学能C.甲装置中铜片表面
在下图所示的装置中 能够发生原电池反应的是( )
在下图所示的装置中,能够发生原电池反应的是()
有A B C三块金属浸泡在稀硫酸中 用导线两两相连要以组成各种原电池。若A B相连 A为负极;B C
有A、B、C三块金属浸泡在稀硫酸中,用导线两两相连要以组成各种原电池。若A、B相连,A为负极;B、C相连,B上有气泡逸出;A、C相连,A极减轻。则三种金属
下列有关原电池叙述正确的是( )A.原电池是将化学能转变成电能的装置B.在原电池中失去电子的一
下列有关原电池叙述正确的是( )A.原电池是将化学能转变成电能的装置B.在原电池中失去电子的一极是阴极C.原电池的两极一定是由活动性不同的两种金属组












