(12分)工业上电解饱和食盐能制取多种化工原料 其中部分原料可用于制备多晶硅。(1)下图是离子交换膜
| (12分)工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。 (1)下图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ;NaOH溶液的出口为 (填字母);精制饱和食盐水的进口为 (填字母);干燥塔中应使用的液体是 。 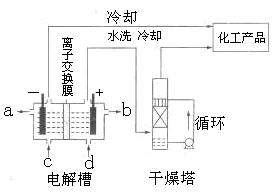 (2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。 ① SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。 ② SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应: 3 SiCl4(g)+2H2(g)+Si(s)  4SiHCl3(g) 4SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为 ______kg。 (3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气 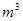 (标准状况)。 (标准状况)。 |
参考解答
| (1)阳极产生的气体是氯气;NaOH溶液的出口为a(填字母);精制饱和食盐水的进口为d(填字母);干燥塔中应使用的液体是浓硫酸。 (2)①化学方程式为SiCl4+2H2+O2 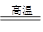 SiO2+4HCl。 SiO2+4HCl。②理论上需消耗纯NaCl的质量为0.35kg。 (3)生成氢气134.4 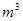 (标准状况)。 (标准状况)。 |
分析:(1)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极发生的方程式为:2Cl--2e-═Cl2↑,阴极:2H++2e-═H2↑;H2、2NaOH在阴极,NaOH溶液的出口为a,Cl2在阳极,精制饱和食盐水从阳极进入,要干燥Cl2需要用酸性干燥剂或中性干燥剂. (2)①SiCl4与H2和O2反应,产物有两种,光导纤维的主要成分是SiO2,H、Cl元素必在另一产物中,H、Cl元素结合成HCl,然后配平即可; ②利用三段分析法,根据平衡时H2与SiHCl3物质的量浓度,求出的起始物质的量,再根据2NaCl+2H2O 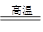 Cl2↑+H2↑+2NaOH,求出理论上消耗纯NaCl的质量; Cl2↑+H2↑+2NaOH,求出理论上消耗纯NaCl的质量;(3)根据得失电子守恒,NaCl转化为NaClO3所失去的电子等于H2O转化为H2所得到的电子,由氯酸钠的质量求出氯酸钠的物质的量,进而求出NaCl转化为NaClO3所失去的电子的物质的量,最后求出生成氢气在标准状况下的体积. 解答:解:(1)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-, 阳极:2Cl--2e-═Cl2↑, 阴极:2H++2e-═H2↑; 总反应为:2NaCl+2H2O  Cl2↑+H2↑+2NaOH, Cl2↑+H2↑+2NaOH,阴极:氢离子放电,产生氢气.致使氢氧根离子浓度增大,钠离子和氢氧根离子的增大都发生在阴极室,所以a出口导出的液体是氢氧化钠溶液; 阳极:氯离子放电,产生氯气,致使钠离子浓度升高,通过阳离子交换膜到达阴极室.所以d入口应加入精制饱和食盐水; 要干燥Cl2需要用酸性干燥剂浓硫酸或P2O5等,中性干燥剂无水CaCl2. (2)①SiCl4与H2和O2反应,产物有两种,光导纤维的主要成分是SiO2,H、Cl元素必在另一产物中,H、Cl元素结合成HCl,然后配平即可. 发生的化学方程式为:SiCl4+2H2+O2 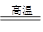 SiO2+4HCl; SiO2+4HCl;②由3SiCl4(g)+2H2(g)+Si(s)  4SiHCl3(g) 4SiHCl3(g)起始量(mol) n 0 变化量(mol) 2x x 4x 平衡量(mol) n-2x 4x 4x=0.020mol/L×20L=0.4mol,x=0.1mol, n-2x=0.140mol/L×20L=2.8mol,n=3.0mol, 由2NaCl+2H2O  Cl2↑+H2↑+2NaOH, Cl2↑+H2↑+2NaOH,2mol 1mol 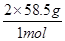 = =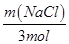 ; m(NaCl)=351g=0.351kg. ; m(NaCl)=351g=0.351kg.(3)由NaCl转化为NaClO3,失去电子数为6,H2O转化为H2,得到的电子数为2, 设产生的H2体积为Vm3, 由得失电子守恒得:6× 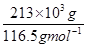 =2× =2×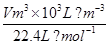 ; ; V=134.4m3. 故答案为:(1)①氯气;a;d;浓硫酸; (2)①SiCl4+2H2+O2 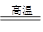 SiO2+4HCl;②0.351; SiO2+4HCl;②0.351;(3)134.4. 点评:本题考查电解、氯碱工业、化学平衡的计算、化学方程式书写、化学计算等知识. |
相似问题
金属镍有广泛应用。粗镍中含有少量Fe Zn Cu Pt等杂质 可用电解法制备高纯度的镍 下列叙述正确
金属镍有广泛应用。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知氧化性Fe2+<Ni2+<Cu2+)A.阳极发生还原反应,
(16分)在一个U形管里盛有氯化铜溶液 并插入两块锌片作电极 按如图连接:(1)如果把开关K接A 该
(16分)在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按如图连接:(1)如果把开关K接A,该装置应是,Zn(2)极是极,电极反应式为。(2)上述
按图装置进行电解(均是惰性电极) 已知A烧杯中装有500 mL20%的NaOH溶液 B烧杯中装有50
按图装置进行电解(均是惰性电极),已知A烧杯中装有500 mL20%的NaOH溶液,B烧杯中装有500 mL pH为6的1 mol·L-1CuSO4溶液。通电一段时间后,在b电
在铁制品上镀上一定厚度的锌层 以下电镀方案中正确的是( )A.锌作阳极 铁制品作阴极 溶液中含
在铁制品上镀上一定厚度的锌层,以下电镀方案中正确的是()A.锌作阳极,铁制品作阴极,溶液中含Fe2+B.锌作阴极,铁制品作阳极,溶液中含Zn2+C.锌作阴
右图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是( )A.从E口逸出的气体是H2B
右图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是()A.从E口逸出的气体是H2B.从B口加入含少量NaOH的水溶液以增强导电性C.标准状况












