如图 研究碳 氮 硫的氧化物的性质对化工生产和环境保护有重要意义.(1)下列措施中 有利于降低大气中
| 如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义. (1)下列措施中,有利于降低大气中的CO2、SO2、NO2浓度的有______.(填字母) a.减少化石燃料的使用,开发新能源 b.使用无氟冰箱,减少氟利昂排放 c.多步行或乘公交车,少用专车或私家车 d.将工业废气用碱液吸收后再排放 (2)为开发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料.一定条件下由CO和H2生产甲醇的化学方程式为______.该反应合成l molCH3OH(1)放出热量131.9kJ,又知2H2(g)+CO(g)+
△H=594.1kJ/mol.请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式:______. (3)硫酸工业生产中,SO2催化氧化生成SO3反应为2SO2+O2?2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图. 根据图示回答下列问题: ①2SO2(g)+O2(g)+O2(g)?2SO3(g)的△H______0 (填“>”或“<”). ②若温度T1、T2时,反应的化学平衡常数分别为K1、K2,则K1______K2;若反应进行到状态D时,v正______v逆(填“>”“<”或“=”). 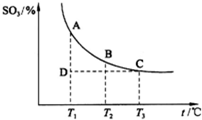 |
参考解答
| (1)a.大量化石燃料的燃烧是二氧化碳的主要来源,减少化石燃料的使用,开发新能源,有利于降低大气中的CO2、SO2、NO2浓度,故a正确; b.氟里昂能促进臭氧地方分解,与大气中的CO2、SO2、NO2浓度无关,故b错误; c.汽车尾气中有多种有害物质,主要污染物是一氧化碳、碳氢化合物、氮的氧化物和烟尘等,故多步行或乘公交车,少用专车或私家车有利于降低大气中的CO2、SO2、NO2浓度,故c正确; d.将工业废气用碱液吸收后再排放能减少CO2、SO2、NO2的排放,故d正确. 故答案为:acd; (2)CO和H2反应生成甲醇,反应方程式为:CO+2H2=CH3OH; 根据液态甲醇燃烧生成二氧化碳和水蒸气,化学方程式为:2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g), 已知:①CO+2H2=CH3OH△H1=+131.9kJ?mol-1 ②2H2(g)+CO(g)+
根据盖斯定律,2×(②-①)得:2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)故△H=2×(△H2-△H1)=-1452kJ?mol-1, 故热化学方程式为:2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1452kJ?mol-1, 故答案为:CO+2H2=CH3OH;2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1452kJ?mol-1; (3)①由图可知,温度越高SO3的含量越低,即升高温度平衡向逆反应移动,所以正反应是放热反应,△H<0, 故答案为:<; ②该反应是一个放热反应,升高温度,平衡向逆反应方向移动,所以生成物的浓度减小,反应物的浓度增大,平衡常数减小,所以K1>K2;D状态相对于A状态,三氧化硫的含量较小,要使该反应达到平衡状态,该反应必须向正反应方向移动,所以正反应速率大于逆反应速率. 故答案为:>;>. |
相似问题
化学反应N2+3H2=2NH3的能量变化图所示 该反应的热化学方程式是( )A.N2(g)+3H2
化学反应N2+3H2=2NH3的能量变化图所示,该反应的热化学方程式是( )A.N2(g)+3H2(g)?2NH3(l)△H=2(a-b+c)kJ molB.N2(g)+3H2(g)?2NH3(l
4P(红磷s) P4(白磷s);△H=+17kJ?mol-1根据以上方程式 下列推论正确的是( )
4P(红磷s)P4(白磷s);△H=+17kJ?mol-1根据以上方程式,下列推论正确的是( )A.当lmol白磷完全转变成红磷时放出17kJ热量B.正反应是一个放热反应
已知在101kPa时 C(石墨) H2和CO的燃烧热分别为393.5kJ/mol 285.8kJ/m
已知在101kPa时,C(石墨)、H2和CO的燃烧热分别为393 5kJ mol、285 8kJ mol和282 8kJ mol.现有H2和CO组成的混合气体112L(标况),经充分燃烧后,放出
写出下列热化学方程式: (1)SiH4是一种无色气体 遇到空气能发生爆炸性自燃 生成SiO2(s)和
写出下列热化学方程式: (1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2(s)和H2O(l);已知室温下2gSiH4自燃放出热量89 2kJ,其热化学方程
某同学发现在灼热的煤炭上洒少量水 煤炉中会产生淡蓝色火焰 煤炭燃烧更旺 因此该同学得出结论“煤炭燃烧
某同学发现在灼热的煤炭上洒少量水,煤炉中会产生淡蓝色火焰,煤炭燃烧更旺,因此该同学得出结论“煤炭燃烧时加少量水,可使煤炭燃烧放出更多的热量.”












