在温度为373K时 将0.100mol无色的N2O4气体放入1L抽空的密闭容器中 立刻出现红棕色 直
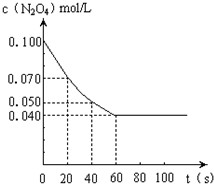
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4  2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间) (1)计算在20至40秒时间内,NO2的平均生成速率为______mol?L-1?S-1. (2)该反应的化学平衡常数表达式为K=______. (3)下表是不同温度下测定得到的该反应的化学平衡常数.
 |
参考解答
(1)在20至40秒时间内,c(N2O4)=
由方程式可知:c(NO2)=2×c(N2O4)=2×0.001mol/(L?s)=0.002mol/(L?s),故答案为:0.002; (2)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,在N2O4  2NO2中,k=
故答案为:
(3)由表中数据可知,温度升高,平衡常数增大,则说明升高温度,平衡向正反应方向移动,则正反应为吸热反应, 故答案为:吸热. |
相似问题
下列说法错误的是 [ ]A.对于反应C(s)+CO2(g)2CO(g) (正反应吸热) 升高
下列说法错误的是 [ ]A.对于反应C(s)+CO2(g)2CO(g) (正反应吸热),升高温度会加快化学反应速率B.合成氨反应中,当3v(NH3)正=2v(H2)逆时,反应达到
如图纵坐标为反应物的转化率α 横坐标为温度(t℃) 下列符合此图情况的反应是( )A.C(s)+C
如图纵坐标为反应物的转化率α,横坐标为温度(t℃),下列符合此图情况的反应是( )A.C(s)+CO2(g)2CO(g);正反应吸热B.H2(g)+Br2(g)2HB
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g) △H<0.在恒温条件下将一定量NO
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g),△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化
在一定温度下 反应A2(气)+B2(气)2AB(气)达到平衡的标志是[ ]A.单位时间生成n
在一定温度下,反应A2(气)+B2(气)2AB(气)达到平衡的标志是[ ]A.单位时间生成n mol的A2同时生成n mol的AB B.容器内的总压强不随时间变化 C.单位
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g) 其他条件不变 在300
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说












