下列溶液中各离子的浓度关系不正确的是( )A.0.1 mol·L-1CH3COONa溶液中:c(C
下列溶液中各离子的浓度关系不正确的是( )
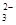 )>c(HCO )>c(HCO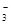 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
参考解答
| CD |
试题分析:A、物料守恒,正确;B、混合得到NaHCO3,质子守恒,正确;C、此混合溶液中存在HCN电离平衡和NaCN水解平衡,溶液为碱性,以水解平衡为主,故c(HCN)>c(Na+>c(CN-)> c(OH-),错误; D、0.3mol NaOH通入0.2mol CO2,产物为同浓度的Na2CO3和NaHCO3,其中存在水解和电离平衡,其中以Na2CO3第一步水解为主,故有c(Na+)> c(HCO 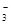 )>c(CO )>c(CO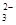 )> c(OH-)>c(H+),错误。 )> c(OH-)>c(H+),错误。 |
相似问题
下列电离方程式中 错误的是( )A.H2CO3?H++HCO3- HCO3-?H++CO32
下列电离方程式中,错误的是( )A.H2CO3?H++HCO3-HCO3-?H++CO32-B.H2SO4=2H++SO42-C.NaHCO3=Na++H++CO32-D.CH3COOH?H++CH3COO-
常温下 向20.00 mL 0.100 mol·L-1CH3COONa溶液中逐滴加入0.100 mo
常温下,向20 00 mL 0 100 mol·L-1CH3COONa溶液中逐滴加入0 100 mol·L-1盐酸,溶液的pH与所加入盐酸体积的关系如图所示(不考虑挥发)。下列说法正
物质在水中可能存在电离平衡 盐的水解平衡和沉淀的溶解平衡。请根据所学知识回答下列问题:(1)NaHC
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡。请根据所学知识回答下列问题:(1)NaHCO3溶液中共存在7种微粒,它们是Na+、HCO、H+、CO、H
化合物HIn在水溶液中因存在以下电离平衡 故可用作酸碱指示剂: HIn(aq)(红色)H+(aq)+
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂: HIn(aq)(红色)H+(aq)+In-(aq)(黄色)浓度为0 02 mol L的下列各溶液:①盐酸;②
常温下 下列说法不正确的是A.等体积 等物质的量浓度的NaCl(aq) 离子总数大于NaClO(aq
常温下,下列说法不正确的是A.等体积、等物质的量浓度的NaCl(aq) 离子总数大于NaClO(aq)中离子总数B.pH=3的硫酸溶液中水的电离程度等于pH=11的氨水溶












