(14分)某研究性学习小组的同学探索工业含铝 铁 铜合金废料的再利用 甲同学设计的实验方案如下:请回
(14分)某研究性学习小组的同学探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下: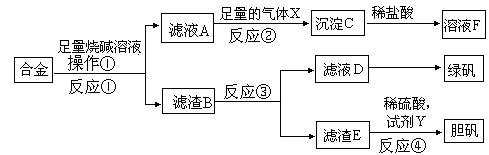 请回答: (1)写出反应②的离子反应方程式__________________________________________。 (2)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,反应④的总化学方程式是_____________________________________。 (3)乙同学在甲同学方案的基础上提出用滤渣B来制备 FeCl3?6H2O晶体,是将所得氯化铁溶液用加热浓缩、降温结晶法制得FeCl3?6H2O晶体,而不用直接蒸发结晶的方法来制得晶体的理由是__________________ (4)丙同学设计如下方案测定甲同学所制得的绿矾晶体中结晶水含量,其方法过程如下 ①称取mg己研细的新制得的绿矾晶体,称量的方法是___________ a.直接将晶体放置于天平托盘上所垫的纸片上称量 b.将晶体置于干燥的坩埚中,然后再按a中操作进行称量 c.将晶体置于己准确称量的干燥坩埚中,然后再按a中操作进行称量 ②在氮气流环境中加热坩埚中晶体使其失去全部结晶水后再停止加热,并仍在氮气流环境下冷却。放在氮气流中加热与冷却的原因是____________________________ ③将坩埚放在天平上进行称量,称得质量为n1g ④重复②、③的操作,称得的质量为n2g,表明不需要再加热再称量的依据是________ ⑤下表数据来是该同学实验报告中的数据,试求出晶体中X=_______
|
参考解答
| (1)AlO2- + CO2 + 2H2O= Al(OH)3↓+ HCO3- (2)Cu + H2O2 + H2SO4 + 3H2O = CuSO4·5H2O或Cu+H2O2 + H2SO4 = CuSO4 + 2H2O (3)因为氯化铁是强酸弱碱盐水解生成氢氧化铁和盐酸,加热蒸干时使HCl 挥发造成水解进行到底,因此得不到FeCl3?6H2O晶体 (4)①c (2) ②防止加热中Fe2+被氧化;③n1-n2≤0.1g, ④7 |
| 三种金属中只有铝能与碱反应生成NaAlO2、通过足量CO2后生成Al(OH)3溶液与NaHCO3。易知E是铜,铜与稀硫酸不反应,故Y有较强的氧化性,结合其为液体知为H2O2;D是FeSO4,可用NaOH 来检验Fe2+。FeCl3是挥发性酸的弱碱盐,直接加热盐溶液时能促使水解进行到底。 应先称量坩埚质量,再称坩埚与药品质量和;亚铁盐在温度较高的条件很易被空气氧化,故应放在氮气流中进行实验;当再次称量数据与第n1相差不超过0.1g时表明符合要求。因2、3两次称量结果相近而第一次与另外两次相差较大,故用2、3两次称量结果的平均值进行计算。 |
相似问题
(13分)根据要求完成下列各小题实验目的。(a b为弹簧夹 加热及固定装置已略去) (1)验证
(13分)根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去) (1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸
(12分)某化学兴趣小组为了探索铝电极在原电池中的作用 设计并进行了以下一系列实验 实验结果记录如下
(12分)某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:编号电极材料电解质溶液电流指针偏转方向1Mg
小张用白纸和无色溶液给表弟写了一封“无字”信 表弟接到信拆开一看觉得很愕然 但沉思一下便明白小张的意
小张用白纸和无色溶液给表弟写了一封“无字”信,表弟接到信拆开一看觉得很愕然,但沉思一下便明白小张的意思。经过用另一溶液简单处理后,表弟看到了一
(每空2分 共12分)某校化学研究性学习小组的同学在学习了金属的知识后 为了解Cu的常见化合物性质
(每空2分,共12分)某校化学研究性学习小组的同学在学习了金属的知识后,为了解Cu的常见化合物性质,运用类比学习的思想提出如下的问题,探究。请你协助
(14分)某学习小组的同学在学习了Na2CO3 NaHCO3的性质后 了解到它们都能与盐酸反应产生C
(14分)某学习小组的同学在学习了Na2CO3、NaHCO3的性质后,了解到它们都能与盐酸反应产生CO2气体,那么如何鉴别Na2CO3和NaHCO3呢?带着这样的疑问,他们












