某校研究性学习小组同学在实验时把一定量的SO2通入装有一定浓度BaCl2溶液的试管中 出现了白色浑浊
| 某校研究性学习小组同学在实验时把一定量的SO2通入装有一定浓度BaCl2溶液的试管中,出现了白色浑浊物。 ⑴实验小组的同学查阅了工具书上的相关数据,经过计算推导得出:即使把SO2通入BaCl2溶液中至饱和,也不可能生成BaSO3,故白色浑浊物只能是BaSO4。你认为所查阅的数据为: SO2的溶解度、SO2饱和溶液中各离子的浓度以及_______________。 ⑵小组同学对白色浑浊物成分及产生原因进行了各种合理的假设,并分别设计实验验证假设如下: |
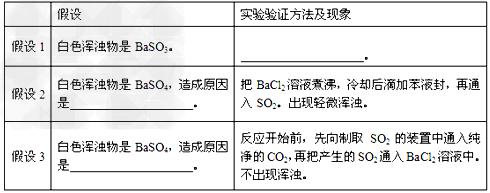 |
| 请把上表填充完全。 ⑶写出在验证假设2的实验时,溶液中发生的反应的化学方程式:________________、 _______________; ⑷请你再提供一种假设。白色浑浊物是BaSO4,造成原因是________________。 |
参考解答
| ⑴BaSO3的溶度积或BaSO3的溶解度 ⑵假设1:在白色浑浊物中加入过量盐酸,变澄清;假设2:BaCl2溶液中溶解的氧气把亚硫酸氧化成硫酸;假设3:SO2中混有空气,把亚硫酸氧化成硫酸 ⑶2SO2 +O2 +2H2O = 2H2SO4或SO2 +H2O =H2SO3、2H2SO3 + O2=2H2SO4;H2SO4 + BaCl2= BaSO4↓+2HCl ⑷BaCl2溶液中混有Ba(NO)3、HNO3、H2O2、Fe3+等均可 |
相似问题
阅读分析材料 完成下列各题: 某同学做同主族元素性质的相似性 递变性实验时 自己设计了一套实验方案
阅读分析材料,完成下列各题: 某同学做同主族元素性质的相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的 “实
某化学兴趣小组欲研究一种镁铝合金 以下是部分实验。请完成填空。 【实验一】从镁铝合金片上剪下一小块
某化学兴趣小组欲研究一种镁铝合金,以下是部分实验。请完成填空。 【实验一】从镁铝合金片上剪下一小块,先称重,然后投到盛有10 mL 10 mol·L-1 N
下面的装置是仿照工业上制备硫酸的工艺流程设计出来的 用于探究工业上为何采用98.3%的浓硫酸吸收三氧
下面的装置是仿照工业上制备硫酸的工艺流程设计出来的,用于探究工业上为何采用98 3%的浓硫酸吸收三氧化硫。 请回答下列问题:(1)写出沸腾炉内煅烧黄铁
下图是探究铜丝与过量浓硫酸的反应下列叙述不正确的是[ ]A.上下移动①中铜丝可控制SO2的量
下图是探究铜丝与过量浓硫酸的反应下列叙述不正确的是[ ]A.上下移动①中铜丝可控制SO2的量 B.②中品红溶液褪色 C.③中石蕊溶液变红色 D.为确认Cu
为证明Fe3+具有较强的氧化性 甲同学做了如下实验:将Cu片放入Fe(NO3)3 溶液中 观察到Cu
为证明Fe3+具有较强的氧化性,甲同学做了如下实验:将Cu片放入Fe(NO3)3 溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较












