硫酸亚铁蓉易被氧化 而硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O]较稳定 常用于代替硫
| 硫酸亚铁蓉易被氧化,而硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O]较稳定,常用于代替硫酸亚铁作还原剂。 现以铁屑为主要原料制备硫酸亚铁铵晶体,其反应如下: Fe+H2SO4(稀) FeSO4+(NH4)2SO4+6H2O 步骤l:在盛有适量铁屑的锥形瓶审加入某种试剂除去油污,加热,充分反应后过滤、洗涤、干燥、称量,铁屑质量为  。 。步骤2:将处理过的铁屑加入到一定量的稀H2SO4中,加热至50℃—80℃充分反应,趁热过滤并用少量热水洗涤,滤液及洗涤液都转移至蒸发皿中。滤渣于燥后称重,剩余铁屑质量为 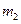 。 。步骤3:准确称取所需质量的硫酸铵晶体加入“步骤2”的蒸发皿中,搅拌使之溶解,缓缓加热一段时间,将其冷却气结晶、过滤。用无水乙醇洗涤晶体并自然干燥,称量所得晶体质量为 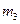 。 。回答下列问题: (1)能够甩于除去铁屑表面油污的试剂是 (填字母)。
步骤2中趁热过滤的目的是 。 (3)硫酸亚铁在潮湿的空气中易被氧化生成一种物质(碱式硫酸铁),该反应的化学方程式为 。 (4)铁屑表面常有少量的铁锈(Fe2O3· 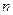 H2O),对FeSO4的制备 (填“有”、“无”)影响,理由是(用离子方程式回答) 。 H2O),对FeSO4的制备 (填“有”、“无”)影响,理由是(用离子方程式回答) 。(5)若忽略铁锈的影响,上述实验中硫酸亚铁铵晶体的产率为 。 (6)请设计一个简单的实验,检验硫酸亚铁铵晶体中含有结晶水(简述实验操作、现象和结论)。 。 |
参考解答
| (1)AB(2分) (2)玻璃棒、烧杯、漏斗(2分) 避免FeSO4因结晶而造成损失(1分) (3)4FeSO4+O2+2H2O (4)无(1分) Fe2O3+6H+ 2Fe3++Fe (5) 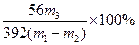 (2分) (2分)(6)取少量硫酸亚铁铵晶体于试管中,用酒精灯加热,在试管品有液体(水珠)生成,说明其中含有结晶水。(2分) |
| 略 |
相似问题
(8分)铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时 观察到铁完全溶解
(8分)铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。请你协助他们探究所得气体的成
一元硬币的外观有银白色的金属光泽 一些同学推测它可能是铁制成的。在讨论时 有同学提出:“我们可以先拿
一元硬币的外观有银白色的金属光泽,一些同学推测它可能是铁制成的。在讨论时,有同学提出:“我们可以先拿磁铁来吸一下。”就这一过程而言,属于科学探
某活动课程小组拟用50mLNaOH溶液吸收CO2气体 制备Na2CO3溶液。为了防止通入的CO2气体
某活动课程小组拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:此方案第一步的实验装置如下
为了制得氯气并探究氯气的一些化学性质 某学生用如图所示装置进行有关实验 打开A的玻璃塞 将A中浓盐酸
为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中。试回答:(1)
(8分)为了探究铁与氯气反应制取氯化铁的实验 某同学甲设计了如下的实验方案。其实验装置如下图 加热装
(8分)为了探究铁与氯气反应制取氯化铁的实验,某同学甲设计了如下的实验方案。其实验装置如下图,加热装置省略。已知:氯化铁易溶于水,熔、沸点低,受热












