某化学课外兴趣小组探究铜与浓硫酸的反应情况。甲 乙 丙三位同学进行了下列实验:取12.8 g铜片和2
| 某化学课外兴趣小组探究铜与浓硫酸的反应情况。甲、乙、丙三位同学进行了下列实验:取12.8 g铜片和20 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余外,同时根据所学的知识认为还有较多的硫酸剩余。 (1)为什么较多的余酸不再与铜片继续反应?简述理由:________________。可以证明有余酸的实验方案是__________(填字母)。 a.再加入铁粉 b.再滴入BaCl2溶液 c.再加入银 d.再滴入Na2CO3溶液 (2)甲同学设计求余酸浓度的实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是 ________(填字母)。 a.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称量 b.将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、 干燥、称量沉淀 c.用排水法测定其产生气体的体积(折算成标准状况) d.用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况) (3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量。在反应后的溶液中加蒸馏水稀释至100 mL,加入足量Na2S溶液,充分反应后,过滤、洗涤、干燥、称量沉淀。请写出生成沉淀的离子方程式: ___________________________。 (4)根据甲、乙两同学的实验方案,除测算产生气体的物质的量或反应掉的铜的物质的量外,尚缺少的测量数据是________。 (5)丙同学提出甲、乙两同学的实验方案较复杂,为此他设计了下列较为简易的实验方案:取出反应后的铜片,进行洗涤、干燥、称量。若称得剩余铜片的质量为W g,测得反应后溶液的体积为V mL,请计算剩余硫酸的物质的量浓度=________mol/L(用含W、V的代数式表示)。 |
参考解答
| (1)铜片过量,随着反应的进行,硫酸逐渐变稀,氧化性减弱;ad (2)ac (3)Cu2++S2-==CuS↓ (4)反应后溶液的体积 (5) 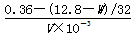 |
相似问题
某化学研究性学习小组设想探究铜的常见化学性质 过程设计如下: [提出猜想] 问题1:在周期表中 铜与
某化学研究性学习小组设想探究铜的常见化学性质,过程设计如下: [提出猜想] 问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性
化学兴趣小组在实验中发现:将锌粒放入CuSO4溶液中一段时间 锌粒表面附着了一层松散的黑色粉末状物质
化学兴趣小组在实验中发现:将锌粒放入CuSO4溶液中一段时间,锌粒表面附着了一层松散的黑色粉末状物质,而不是预期的红色物质。通过查阅资料和讨论,大家
某兴趣小组通过实验探究溶解铜的方法和本质。(1)在热水浴中进行3个实验 部分实验报告如下表所示。 ①
某兴趣小组通过实验探究溶解铜的方法和本质。(1)在热水浴中进行3个实验,部分实验报告如下表所示。 ①实验I、Ⅱ的目的是____; ②实验Ⅲ中反应的本质是
为测定某有机化合物A的结构 进行如下实验:I分子式的确定。(1)将一定量的有机物A置于氧气流中充分燃
为测定某有机化合物A的结构,进行如下实验:I分子式的确定。(1)将一定量的有机物A置于氧气流中充分燃烧,实验测得:生成5 4 g H2O和8 8 g CO2,消耗
科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。 I.四种制取Cu2O的方法:(1)火还原法
科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。 I.四种制取Cu2O的方法:(1)火还原法:用炭粉在高温条件下还原CuO。 (2)用葡萄糖[CH2OH(CHOH)4












