为探究乙烯与溴的加成反应:甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯 将生成的气体直
| 为探究乙烯与溴的加成反应:甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量浓硫酸的还原气体,由此他提出必须先除去,再与溴水反应. 请你回答下列问题: (1)甲同学设计的实验______(填“能”或“不能”)验证乙烯与溴水发生了加成反应,理由是______. (2)乙同学推测此乙烯中必定含有的一种杂质气体,它与溴水反应的化学方程式是______.在验证过程中必须全部除去,为此乙同学设计了如图所示的实验装置: ①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是Ⅰ______;Ⅱ______;Ⅲ______;Ⅳ______; (选填序号). A.品红溶液B.NaOH溶液C.浓硫酸D.酸性KMnO4溶液 ②乙设计的实验中能确定生成了乙烯的现象是______. (3)为验证乙烯与溴水的反应是加成反应而不是取代反应,丙同学提出可将上述乙除杂后的气体通入溴水中,用pH试纸测反应后溶液的酸碱性,你认为是否合理______(填合理、不合理),理由是______. (4)乙烯通入溴水中,观察到的现象是______;其反应方程式为______. 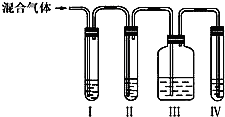 |
参考解答
| (1)乙醇和浓硫酸反应,在一定条件下可以生成乙烯、乙醚,同时可能生成二氧化硫等还原性气体,使酸性高锰酸钾溶液褪色,对乙烯的检验造成干扰,所以甲同学的实验不能说明乙烯与溴水发生加成反应, 故答案为:不能;乙醇和浓硫酸为原料制取乙烯时,生成的气体中可能含有二氧化硫,二氧化硫也能使溴水褪色; (2)二氧化硫、溴水发生氧化还原反应生成硫酸和氢溴酸,反应方程式为2H2O+Br2+SO2=H2SO4+2HBr,故答案为:2H2O+Br2+SO2=H2SO4+2HBr; ①验证过程中必须排除二氧化硫的干扰,所以先除去二氧化硫,I中盛放品红溶液检验二氧化硫、II中盛放氢氧化钠溶液除去二氧化硫、III中盛放品红溶液检验二氧化硫是否除尽,IV中盛放酸性高锰酸钾检验乙烯的性质,故答案为:A;B;A;D; ②III中溶液不褪色,说明剩余气体中不含二氧化硫,IV中酸性高锰酸钾溶液褪色,说明乙烯能使酸性高锰酸钾褪色,故答案为:III中品红溶液不褪色,IV中酸性高锰酸钾溶液褪色; (3)若乙烯和溴发生取代反应,则该反应中有溴化氢生成,用pH试纸测反应后溶液应该呈酸性,如果溶液没有呈酸性,则证明发生加成反应,所以丙同学的设计合理, 故答案为:合理;若发生取代反应,必有溴化氢生成,溶液呈酸性; (4)溴和乙烯发生加成反应生成1,2-二溴乙烷,且1,2-二溴乙烷密度较大,所以下层有无色油状液体生成,反应方程式为:CH2=CH2+Br2→CH2BrCH2Br, 故答案为:溴水褪色,下层有无色油状物生成;CH2=CH2+Br2→CH2BrCH2Br. |
相似问题
下列关于对燃烧现象的认识中 不正确的是( )A.燃烧一定是氧化还原反应B.燃烧一定发光放热C.燃烧
下列关于对燃烧现象的认识中,不正确的是( )A.燃烧一定是氧化还原反应B.燃烧一定发光放热C.燃烧一定是化学反应D.燃烧一定有氧气参与
如图所示实验装置或操作不符合实验要求的是( )A.石油分馏B.灼烧干海带C.用CCl4提取碘水中的
如图所示实验装置或操作不符合实验要求的是( )A.石油分馏B.灼烧干海带C.用CCl4提取碘水中的碘D.冶炼金属铁
对下列实验过程的评价 正确的是( )A.某固体中加入稀盐酸 产生了无色气体 证明该固体中一定含有碳
对下列实验过程的评价,正确的是( )A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐B.验证烧碱溶液中是否含有Cl-,先加过量稀
下面实验操作可以实现实验目的是( )A.将温度计水银球插入蒸馏烧瓶的石油中来蒸馏石油B.将SO2通
下面实验操作可以实现实验目的是( )A.将温度计水银球插入蒸馏烧瓶的石油中来蒸馏石油B.将SO2通入酸性KMnO4溶液中,溶液褪色,证明SO2具有漂白性C
研究有机物一般经过以下几个基本步骤:分离 提纯→确定实验式→确定分子式→确定结构式 以下用于研究有机
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是 [ ]A.燃烧法是研究确定有












