(12分)甲醇作为新型汽车动力燃料 工业上可由CO和H2合成。该反应的热化学方程式:该反应的原
(12分)甲醇作为新型汽车动力燃料,工业上可由CO和H2合成。该反应的热化学方程式: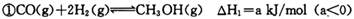 该反应的原料CO和H2本身可作为燃料,它们的热化学方程式为: 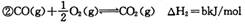 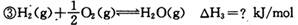 某些化学键的键能数据如下表 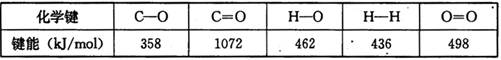 请回答下列问题: (1)反应③中的ΔH3=________kJ/mol (2) CH3OH燃烧生成CO2(g)和H2O(g)的热化学方程式为 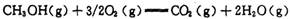 ,该反应的焓变 ,该反应的焓变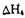 =________kJ/mol (用含a、b的式子表示); =________kJ/mol (用含a、b的式子表示);(3) 若降低温度,反应①的化学平衡常数K值将________ (填“增大”、“减小”或“不变”); (4) 甲醇一空气电池是一种髙效、低污染质子交换腆燃料电池,电池总反应为 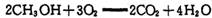 。甲醉在催化剂作用下提供质子和电子。右图为该电池的示意图,则电极d上发生的电极反应式为________________。 。甲醉在催化剂作用下提供质子和电子。右图为该电池的示意图,则电极d上发生的电极反应式为________________。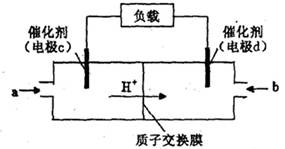 |
参考解答
| (1)- 239;(2)b-a-478;(3) 增大;(4)O2+4e-+4H+=2H2O。 |
| 本题考查化学反应热的计算、化学平衡常数比较和电化学知识。 (1)反应热可根据反应和生成物的键能进行计算,ΔH3=反应键能之和- 生成物键能之和= -436 kJ/mol +(1/2)498 kJ/mol-2×462 kJ/mol='-' 239kJ/mol; (2) 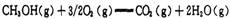 可由②-①-2×③得ΔH4=ΔH2-ΔH1-2ΔH3='(b-a-478)' kJ/mol; 可由②-①-2×③得ΔH4=ΔH2-ΔH1-2ΔH3='(b-a-478)' kJ/mol;(3) 反应①正反应是放热反应,若降低温度,平衡向正反应方向移动,平衡常数K值将增大; (4) 从该电池的示意图H+的移动方向可以看出,电极d是该电池的正极,发生还原反应,电极反应式为O2+4e-+4H+=2H2O。 |
相似问题
组成生命细胞的11种宏量元素(约占人体总质量的99.97%) 全部位于周期表的前20号。其中组成人体
组成生命细胞的11种宏量元素(约占人体总质量的99 97%),全部位于周期表的前20号。其中组成人体蛋白质、脂肪、碳水化合物和核酸的主要有6种元素。(1)
下列过程中 共价键被破坏的是
下列过程中,共价键被破坏的是()A.碘升华 B.HI气体受热分解C.食盐熔化D.金属钠熔化
沸腾时只需克服范德华力的物质是( )A.水B.CCl4C.氨水D.水银
沸腾时只需克服范德华力的物质是()A.水B.CCl4C.氨水D.水银
下列各组物质中 化学键类型不同的是( )A.NaCl和HNO3B.H2O和NH3C. CaF2和C
下列各组物质中,化学键类型不同的是( )A.NaCl和HNO3B.H2O和NH3C. CaF2和CsClD.CCl4和Na2O
下列关于杂化轨道的叙述中 不正确的是A.分子中中心原子通过sp3杂化轨道成键时 该分子不一定为正四面
下列关于杂化轨道的叙述中,不正确的是A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构B.杂化轨道只用于形成σ键或用于容纳未参与












