应4NH3+5O2 4NO+6H2O在5L的密闭容器中进行 半分钟后 NO的物质的量增加了0.3mo
应4NH3+5O2 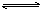 4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则下列反应速率正确的是 4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则下列反应速率正确的是
|
参考解答
| D |
| v(NO)=0.3mol÷5L÷30s='0.' 002 mol/(L· s) A.v(O2)=0.002mol/(L· s)×5/4=0.0025mol/(L· s) B.v(NO)=0.002mol/(L· s) C.v(H2O)=0.002mol/(L· s)×6/4=0.003mol/(L· s) D.v(NH3)=0.002mol/(L· s)= v(NO) 选D。 |
相似问题
反应4NH3+5O2 4NO+6H2O在5 L的密闭容器中进行 半分钟后 NO的物质的量增加了0.3
反应4NH3+5O24NO+6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0 3 mol,则此反应的平均速率(表示反应物的消耗速率或生成物的生成速率)
在2L密闭容器中 发生如下反应:3A(g)+B(g) →C(g)+D(g) 若开始时加入的A和B都是
在2L密闭容器中,发生如下反应:3A(g)+B(g) →C(g)+D(g),若开始时加入的A和B都是4mol,在前10s内A的平均速率为0 12mol (L·s),则10s时容器内B的物质的
在容积不变的密闭容器中存在如下反应: 2SO2(g)+O2(g)2SO3(g);△H
在容积不变的密闭容器中存在如下反应: 2SO2(g)+O2(g)2SO3(g);△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确
(6分)大理石与盐酸反应的反应速率如右图所示 已知该反应为放热反应。(1)写出该反应的离子反应方程式
(6分)大理石与盐酸反应的反应速率如右图所示,已知该反应为放热反应。(1)写出该反应的离子反应方程式:。(2)反应开始时反应速率加快的原因是:。(
(9分)将等物质的量A B气体 置于容积为2L的密闭容器中发生反应 当反应进行到8s末 达到该反应的
(9分)将等物质的量A、B气体,置于容积为2L的密闭容器中发生反应,当反应进行到8s末,达到该反应的限度,测得A的物质的量减少0 6mol,B的物质的量减少0












