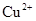在下图所示的原电池中 下列说法正确的是A.Zn为负极 Cu为正极B.正极反应为 Zn - 2e- =
在下图所示的原电池中,下列说法正确的是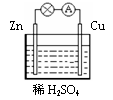
|
参考解答
| A |
铜锌原电池,活泼金属作负极,不活泼金属作正极,A正确;正极得到电子,电极反应方程式为2H++2e- ='=' H2,,B错误;负极的电极反应式为Zn - 2e- ='=' 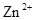 ,C错误;原电池是将化学能转化为电能,D错误;所以答案选A。 ,C错误;原电池是将化学能转化为电能,D错误;所以答案选A。 |
相似问题
(13 分)(1)CuSO4溶液是中学化学及工农业生产中常见的一种试剂。某同学利用CuSO4溶液 进
(13 分)(1)CuSO4溶液是中学化学及工农业生产中常见的一种试剂。某同学利用CuSO4溶液,进行以下实验探究。①图一是根据反应Zn + CuSO4 =" Cu" +
关于锌 铜和稀H2SO4构成的原电池的下列说法中正确的是 A.锌溶解的速率比锌直接与同浓度硫酸反应
关于锌、铜和稀H2SO4构成的原电池的下列说法中正确的是 A.锌溶解的速率比锌直接与同浓度硫酸反应快 B.电子从铜片经导线流向锌片C.负极的反应式为2
下列各组的电极材料和电解液 不能组成原电池的是( )A.铜片 石墨棒 硫酸铁溶液B.铜片 石墨棒
下列各组的电极材料和电解液,不能组成原电池的是()A.铜片、石墨棒,硫酸铁溶液B.铜片、石墨棒,硫酸铜溶液C.锌片、铜片,稀盐酸D.铜片、银片,硝
铜锌原电池(如图)工作时 下列叙述正确的是 A正极反应为:Zn—2e-=Zn2+
铜锌原电池(如图)工作时,下列叙述正确的是A正极反应为:Zn—2e-=Zn2+ B电池反应为:Zn+Cu2+=Zn2+ +CuC 在外电路中,电子从正极流向负极D 盐桥中的K+移向ZnSO4溶液
下列说法正确的是A.牺牲阴极的阳极保护法是应用电解原理防止金属的腐蚀B.CO的标准燃烧热是283.0
下列说法正确的是A.牺牲阴极的阳极保护法是应用电解原理防止金属的腐蚀B.CO的标准燃烧热是283 0 kJ·mol-1,则2CO2(g) =2CO(g)+O2(g)反应的 ΔH=