现有三个反应:反应① Fe(s)+H2O(g)FeO(s)+H2(g) △H1 平衡常
| 现有三个反应:反应 ① Fe(s)+H2O(g)  FeO(s)+H2(g) △H1 平衡常数为K1 FeO(s)+H2(g) △H1 平衡常数为K1 反应② CO(g)+H2O(g)  H2(g)+CO2(g) △H2 平衡常数为K2 H2(g)+CO2(g) △H2 平衡常数为K2 反应③ Fe(s)+CO2(g)  FeO(s)+CO(g) △H3 平衡常数为K3 FeO(s)+CO(g) △H3 平衡常数为K3在不同温度下,部分K1、K2的值如下: |
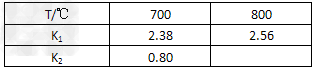 |
| (1)K1的表达式为______;根据反应①、②、③推导出K1、K2、K3的关系式K3=______。 (2)要使反应①在一定条件下建立的平衡右移,可采取的措施有_________。(填字母) A.缩小容器体积 B.降低温度 C.升高温度 D.使用合适的催化剂 E.设法减少H2的量 F.设法减少FeO的量 (3)800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应②,反应过程中测定的部分数据见下表 |
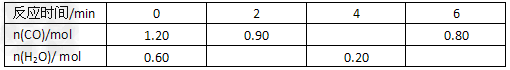 |
| ①反应在2 min内的平均速率为v(H2O)=________________; ②800℃时,K2的值为_______________; ③保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率_______(填“增大”或“减小”或“不变”)。 (4)由以上信息推断反应③正反应方向为________(填“放热”或“吸热”)反应。 (5)在恒温恒压密闭容器中通入CO和H2O各1 mol发生反应②,当反应达到平衡后,维持温度与压强不变,t1时再通入各1 mol的CO和H2O的混合气体,请在下图中画出正(v正)、逆(v逆)反应速率在t1后随时间t变化的曲线图。 |
 |
参考解答
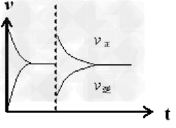
| (1)K1 = c(H2) / c(H2O);K1/K2 (2)CE (3)①0.075 mol·L-1·min-1; ②1;③增大 (4)放热 (5) |
 |
相似问题
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的容器中 发生反应:2SO2+O2
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的容器中,发生反应:2SO2+O22SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器
一定条件下 向一带活塞的密闭容器中充入2 mol SO2和1 mol O2 发生下列反应:2SO2(
一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g)2SO3(g),达到平衡后改变下述条件,SO3平衡浓度不改变的是 [ ]
与甲醇燃料电池相比 乙醇燃料电池具有毒性低 理论能量密度高等优点 因此被广泛认为是更有前途的燃料电池
与甲醇燃料电池相比,乙醇燃料电池具有毒性低、理论能量密度高等优点,因此被广泛认为是更有前途的燃料电池.图是一个乙醇燃料电池工作时的示意图.乙池
下列说法正确的是( )A.电离平衡常数受溶液浓度的影响B.电离平衡常数可以表示弱电解质的相对强弱C
下列说法正确的是( )A.电离平衡常数受溶液浓度的影响B.电离平衡常数可以表示弱电解质的相对强弱C.电离常数大的酸溶液中c(H+)一定比电离常数小
一定温度下 反应N2(g)+3H2(g) 2NH3(g)的反应热和化学平衡常数分别为△H和K 则相
一定温度下,反应N2(g)+3H2(g)2NH3(g)的反应热和化学平衡常数分别为△H和K,则相同温度时反应4NH3(g)2N2(g)+6H2(g)反应热和化学平衡常数为












