(1)下列装置能组成原电池的是______.(填序号)(2)对于锌-铜-稀硫酸组成的原电池装置 当导
(1)下列装置能组成原电池的是______.(填序号)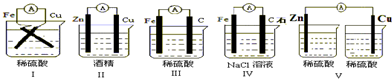 (2)对于锌-铜-稀硫酸组成的原电池装置,当导线中有1mol电子通过时,锌片溶解了______g,铜片上析出______升 H2(标准状况下).电池总反应的化学方程式为______. 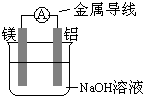 (3)如右图所示装置,若烧杯中溶液为氢氧化钠溶液,则负极为______,总反应方程为______.该装置将______能转化为______能. (4)利用反应:Fe+2Fe3+=3Fe2+设计一个化学电池(电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料. |
参考解答
| (1)II中不能自发的进行氧化还原反应,所以不能构成原电池; V中不能构成闭合回路,所以不能构成原电池,则Ⅰ、Ⅲ、Ⅳ符合原电池构成条件,所以能形成原电池,故选I、III、IV; (2)该原电池中,锌作负极,铜作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子生成氢气,所以电池反应式为:Zn+H2SO4=ZnSO4+H2↑,根据转移电子相等得,锌减少的质量=
故答案为:32.5g,11.2L,Zn+H2SO4=ZnSO4+H2↑; (3)该装置符合原电池的构成条件,所以是原电池,原电池是将化学能转变为电能的装置,铝在碱性溶液中比镁易失电子,所以铝作负极,负极上铝失电子和氢氧根离子反应生成偏铝酸根离子,正极上水得电子生成氢气,所以电池反应式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑, 故答案为:Al,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,化学能、电能; (4)在Fe+2Fe3+=3Fe2+反应中,Fe被氧化,应为原电池的负极,电解反应为:Fe-2e-=Fe2+,Fe3+得电子被还原,应为原电池正极反应,正极材料为活泼性比Fe的金属或非金属材料如碳棒,电解质溶液为含Fe3+离子的溶液,如FeCl3, 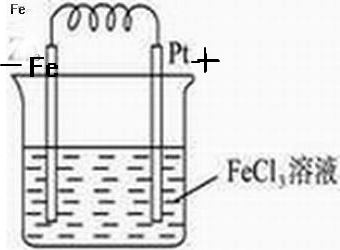 , 故答案为:  . |
相似问题
下列各选项中所述的两个量 前者一定大于后者的是( )A.H3BO3的酸性与H2CO3的酸性B.向
下列各选项中所述的两个量,前者一定大于后者的是()A.H3BO3的酸性与H2CO3的酸性B.向Ag2CrO4浑浊液中加NaCl溶液,有AgCl沉淀生成,Ksp (Ag2CrO4) 与
根据如图 下列判断中不正确的是( )A.通入O2的电极的电极反应式为:O2+2H2O+4e-=4O
根据如图,下列判断中不正确的是( )A.通入O2的电极的电极反应式为:O2+2H2O+4e-=4OH-B.反应一段时间后,甲池中溶液的pH降低C.乙池中电极B上发生
在盛有稀硫酸的烧杯中放入导线连接的锌片和铜片 下列叙述正确的是( )A.正极有O2逸出B.铜片上有
在盛有稀硫酸的烧杯中放入导线连接的锌片和铜片,下列叙述正确的是( )A.正极有O2逸出B.铜片上有H2逸出C.正极附近的SO42-离子浓度逐渐增大D.电子
用NaOH溶液吸收二氧化硫 将所得的混合液进行电解循环再生 这种新工艺叫再生循环脱硫法.其中阴阳膜组
用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是(
(16分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源 具有广泛的开发和应用前景。(1)工
(16分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。(1)工业上合成甲醇的反应原理为:CO(g) + 2H2(g)CH3












