一定温度下 在一固定体积的容器中 通人一定量的CO和H2O 发生如下反应:CO(g)十H2O(g)C
一定温度下,在一固定体积的容器中,通人一定量的CO和H2O,发生如下反应:CO(g)十H2O(g)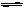 CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是: CO2(g)十H2 (g) △H<0。在850℃时,CO和H2O浓度变化如下左图;若在t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。下列说法正确的是: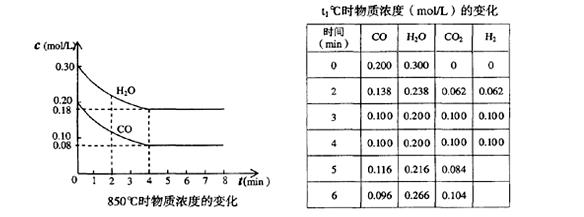
|
参考解答
| B |
试题分析:A、因图中没有CO2的浓度变化曲线,所以只有通过CO 和H2O浓度,通过三段式间接计算CO2的变化浓度,即 CO(g)十H2O(g) 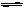 CO2(g)十H2 (g) CO2(g)十H2 (g) 起始浓度(mol/L) 0.2 0.3 0 0 转化浓度(mol/L) 0.12 0.12 0.12 0.12 平衡浓度(mol/L) 0.08 0.18 0.12 0.12 4分钟时浓度不变,达到平衡,则v(CO2)=0.12mol/L÷4min=0.03 mol·L-1·min-1,A不正确; B、观察右表数据,第3分钟时达到平衡,说明达到平衡的时间缩短,速率更快,则温度应该更高,所以B正确; C、根据方程式计量数可知,该反应是体积不变的,即使增大压强,平衡也不移动,而表中数据说明4~5分钟时,CO和H2O的浓度再增大,CO2的浓度再减小,平衡应该是逆向移动,可能的原因是升高温度,C不正确; D、根据方程式可知,该反应的平衡常数表达式K= 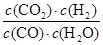 ,850℃时K= ,850℃时K=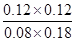 =1。此时(CO2)·c(H2)=2 [c(CO)·c(H2O),即K=2>1。这说明平衡正向移动,则温度降低,应低于850℃,D不正确,答案选B。 =1。此时(CO2)·c(H2)=2 [c(CO)·c(H2O),即K=2>1。这说明平衡正向移动,则温度降低,应低于850℃,D不正确,答案选B。 |
相似问题
在恒温 恒压下 a mol A和b molB在一个容积可变的容器中发生反应:A(g)+2B(g)?2
在恒温、恒压下,amolA和bmolB在一个容积可变的容器中发生反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成nmolC.下列说法正确的( )A.物
下列有关说法正确的是( )A.已知△G=△H-T△S △G <0反应自发进行 2CO(g)
下列有关说法正确的是( )A.已知△G=△H-T△S, △G <0反应自发进行,2CO(g)+2NO(g) =N2(g)+2CO2(g)在温度为298℃时能自发进行,则它的△H>0B
氨的催化氧化过程主要有以下两个反应:(ⅰ)4NH3(g)+5O2(g)4NO(g)+6H2O(g)
氨的催化氧化过程主要有以下两个反应:(ⅰ)4NH3(g)+5O2(g)4NO(g)+6H2O(g) ΔH=-905 5 kJ·mol-1(ⅱ)4NH3(g)+3O2(g)2N2(g)+6H2O(g) ΔH=-1267
合成氨工业对国民经济和社会发展具有重要的意义。哈伯法合成氨需要在20-50MPa的高压和500℃的高
合成氨工业对国民经济和社会发展具有重要的意义。哈伯法合成氨需要在20-50MPa的高压和500℃的高温下,并用铁作为催化剂,氨的转化率为10%-15%。最近美
一定温度下 在2 L密闭容器中发生下列反应:4NO2(g)+O2(g)2N2O5(g);已知该反应的
一定温度下,在2 L密闭容器中发生下列反应:4NO2(g)+O2(g)2N2O5(g);已知该反应的平衡常数:K300 ℃>K350 ℃,且n(NO2)(单位:mol)随时间变化如下表












