影响化学反应速率的因素很多 某课外兴趣小组用实验的方法进行探究。实验一:他们利用Cu Fe Mg和不
| 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。 实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。 (1)甲同学研究的实验报告如下表:
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品是_____________;应该测定的实验数据是________________________。 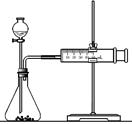 实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。 (1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是______________的影响。 (2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是______。 A、硫酸钾 B、硫酸锰 C、水 D、氯化锰 |
参考解答
| (12分) 实验一:(1)反应物本身的性质对反应速率的关系;(2分) 温度相同;(2分) (2)Mg(或Fe)和0.5mol/L硫酸和2mol/L硫酸;(2分) 测定一定时间产生气体的体积(或者测定一定体积的气体所需时间);(2分) 实验二:(1)催化剂(或硫酸锰或Mn2+的催化作用);(2分) (2)B(2分) |
试题分析:实验一:(1)根据表中的信息得出该同学的实验目的是研究反应物本身的性质对反应速率的关系对反应速率的影响。温度对化学反应速率的影响较大,故根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持温度相同。 (2)根据装置图可以得到,是通过测量生成气体的量来研究浓度对反应速率的影响。故该实验应选用的实验药品是Mg(或Fe)和0.5mol/L硫酸和2mol/L硫酸。应该测定的实验数据是应该测定的实验数据。 实验二:(1)对化学反应速率影响最快的是催化剂,故猜想还可能是催化剂的影响。 (2)选择可以做催化剂的试剂且是生成物,故选B。 点评:影响化学反应速率的外界条件除温度、浓度、压强、催化剂外,还有很多因素可以改变反应速率.如光辐射、超声波、电弧、激光、强磁场、高速研磨、反应物颗粒大小、扩散速率、溶剂等.总之,向反应体系中输入能量,都有可能改变反应速率.外界条件只是影响反应速率,决定化学反应速率的是物质本身的性质。 |
相似问题
用锌片和稀硫酸反应制取氢气时 为加快生成氢气的速率 下列措施不适宜的是A.对该反应体系加热B.加入硝
用锌片和稀硫酸反应制取氢气时,为加快生成氢气的速率,下列措施不适宜的是A.对该反应体系加热B.加入硝酸铜固体C.改用粗锌D.不用锌片,改用锌粉
下列说法合理的是( )A.增加反应物的用量 化学反应速率一定加快B.在等浓度NaCl和Na2CrO4
下列说法合理的是()A.增加反应物的用量,化学反应速率一定加快B.在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,则KSP(AgCl)<KSP(Ag2CrO4
下列各组Na2S2O3溶液跟稀H2SO4反应的实验中 溶液中最先变浑浊的是选项反应温度反 应 物H2
下列各组Na2S2O3溶液跟稀H2SO4反应的实验中,溶液中最先变浑浊的是选项反应温度反应物H2ONa2S2O3H2SO4t(℃)V(mL)c(mol×L-1)V(mL)c(mol×L-1)V(mL)A105
稀硫酸跟过量的铁粉反应时 为了减缓反应速率 且不影响生成H2的总量。下列操作符合的是( )① 加
稀硫酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成H2的总量。下列操作符合的是()① 加Na2O2固体 ② 加H2O③ 加H2C2O4晶体(乙二酸) ④ C
(8分)草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4- + H 2C2O4 + H+ ——M
(8分)草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4- + H 2C2O4 + H+ ——Mn2++ CO2↑+ H2O(未配平)用4 mL 0 001 mol L KMnO4溶液












